“8·12”天津港危化仓库爆炸,造成生命、财产的特大损失。据查危化仓库中存有大量的钠、钾、白磷(P4)、硝酸铵和氰化钠(NaCN)。请回答下列问题:
(1)钠、钾着火,下列可用来灭火的是 。
A. 水 B.干冰 C.细沙 D.泡沫灭火器
(2)白磷有毒能和氯酸溶液发生氧化还原反应:3P4 + 10HClO3 + 18H2O =" 10HCl" + 12H3PO4,该反应的氧化剂是_________,氧化产物是_________,若有1 mol P4参加反应转移电子为_________mol。
(3)NH4NO3为爆炸物,在不同温度下加热分解,可能发生非氧化还原反应,也可能发生氧化还原反应,下列反应一定不可能发生的是 。
A. NH4NO3 → N2 + O2 + H2O B. NH4NO3 → NH3 + HNO3
C. NH4NO3 → O2 + HNO3 + H2O D. NH4NO3 → N2 + HNO3 + H2O
(4)NaCN属于剧毒物质,有多种无害化处理方法。
①H2O2处理法:NaCN + H2O2 — N2↑+ X + H2O,推测X的化学式为 。
②以TiO2为催化剂用NaClO将CN-氧化成为CNO-,CNO-在酸性条件下继续与NaClO反应生成N2、CO2、Cl2等。取浓缩后含CN-的废水与过量NaClO溶液的混合液共200mL(设其中CN-的浓度为0.2 mol·L—1)进行实验。写出CNO-在酸性条件下被NaClO氧化的离子方程式__________________,若结果测得CO2的质量为1.408g,则该实验中测得CN-被处理的百分率为 。
以乙炔或苯为原料可合成有机酸H2MA,并进一步合成高分子化合物PMLA。
I.用乙炔等合成烃C。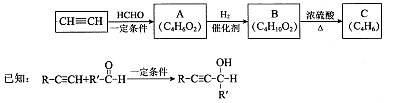
(1)A分子中的官能团名称是、。
(2)A的一种同分异构体属于乙酸酯,其结构简式是。
(3)B转化为C的化学方程式是,其反应类型是。
II.用烃C或苯合成PMLA的路线如下。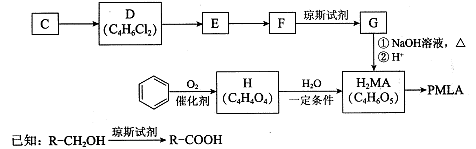
(4)1 mol有机物H与足量NaHC03溶液反应生成标准状况下的C02 44.8L,H有顺反异构,其反式结构简式是。
(5)E的结构简式是。
(6)G与NaOH溶液在加热条件下反应的化学方程式是。
(7)聚酯PMLA有多种结构,写出由H2MA制PMLA的化学方程式(任写一种)。
铬污染主要产生于铬矿的开采和冶炼。工厂排出的铬渣成分为SiO2、 A12O3、MgO、 Fe2O3、Na2Cr2O7等,其中危害最大的化学成分是Na2Cr2O7。已知:① Na2Cr2O7易溶于水,是强氧化剂。② +6价铬易被人体吸收,可致癌;+3价铬不易被人体吸收,毒性小。下面是实验室模拟处理铬渣、消除铬污染的工艺流程如下(部分操作和条件略):
(1)在酸浸过程中,稀H2SO4溶解A12O3的离子方程式是。
(2)过滤1后的滤液中存在如下平衡:Cr2O72-(橙色)+ H2O  2CrO42-(黄色)+ 2H+,此时溶液应呈现的颜色是。
2CrO42-(黄色)+ 2H+,此时溶液应呈现的颜色是。
(3)用FeSO4·7H2O还原 Na2Cr2O7的离子方程式是。
(4)已知:生成氢氧化物沉淀的pH
| 物质 |
Fe(OH)3 |
Al(OH)3 |
Cr(OH)3 |
Fe(OH)2 |
Mg(OH)2 |
| 开始沉淀 |
1.5 |
3.4 |
4.9 |
6.3 |
9.6 |
| 完全沉淀 |
2.8 |
4.7 |
5.5 |
8.3 |
12.4 |
根据表中数据,流程中的a为。
(5)分离滤渣2中物质,发生反应的离子方程式是。
(6)过滤3所得滤液又回流到过滤1所得滤液中,其目的是。
甲醇是一种可再生的优质燃料,用途广泛,研究其作用具有广阔前景。
(1)已知在常温常压下,测得反应的反应热如下:
① 2CH3OH(l)+ 3O2(g)  2CO2(g) +4H2O(g)∆H1= -1275.6 kJ/mol
2CO2(g) +4H2O(g)∆H1= -1275.6 kJ/mol
② 2CO(g) +O2(g)  2CO2(g)∆H2=-566.0 kJ/mol
2CO2(g)∆H2=-566.0 kJ/mol
CH3OH不完全燃烧生成CO和气态水的热化学方程式是。
(2)工业上生产甲醇的反应如下:CO2(g) + 3H2(g)  CH3OH(g)+ H2O(g)∆H = -49 kJ/mol
CH3OH(g)+ H2O(g)∆H = -49 kJ/mol
在某温度下,容积均为1 L的A、B两个容器中,按不同方式投入反应物,保持恒温恒容。容器B中经10 s后达到平衡。达到平衡时的有关数据如下表:
| 容器 |
A |
B |
| 反应物投入量 |
1 mol CO2(g)和3 mol H2(g) |
1 mol CH3OH(g)和1 mol H2O(g) |
| 反应能量变化 |
放出αkJ热量 |
吸收19.6 kJ热量 |
①从反应开始至达到平衡时,容器B中CH3OH的平均反应速率为。
②该温度下,B容器中反应的化学平衡常数的数值为。
③α=。
④下列措施能使容器A中甲醇的产率增大的是。
a.升高温度 b.将水蒸气从体系分离
c.用更有效的催化剂 d.将容器的容积缩小一半
(3)我国科学院化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池。甲醇燃料电池的工作原理如下图所示。
① 该电池工作时,b口通入的物质为。
② 该电池正极的电极反应式为。
A~E五种元素中,除E外均为短周期元素,且原子序数依次增大。它们的原子
结构或性质如下表所示:
| 元素 |
A |
B |
C |
D |
E |
| 结构或性质 |
原子半径最小的元素 |
地壳中含量最多的元素 |
可与B形成阴阳离子个数比为1:2的两种化合物 |
与B同主族 |
单质是生活中最常见的金属,可被磁铁吸引 |
(1)元素D在周期表中的位置为。
(2)C与B形成原子个数比为1∶1的化合物中,含有的化学键类型为。
(3)化合物甲、乙是由A、B、C、D四种元素中的三种组成的强电解质,且两种物质水溶液均显碱性。若甲能抑制水的电离,乙能促进水的电离,则化合物甲的电子式为;乙的化学式是。
(4)以E构成的单质为Y极,碳棒为X极,在6 mol/L的NaOH溶液中进行电解,制取高效净水剂Na2YO4(溶液呈紫红色)。其装置如图。电解过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色,且Y电极变细;电解液澄清。Y极发生的电极反应为:4OH--4e- 2H2O+O2↑和。若在X极收集气体672 mL,在Y极收集气体168 mL(均已折算为标况下体积),则Y电极质量减少g。
2H2O+O2↑和。若在X极收集气体672 mL,在Y极收集气体168 mL(均已折算为标况下体积),则Y电极质量减少g。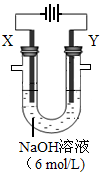
(5)Se是人体必备的微量元素,与B、D同一主族。Se的原子序数为34,且B、D、Se元素气态单质分别与H2反应生成1 mol气态氢化物的反应热如下:
a.+ 29.7 kJ/mol b.-20.6 kJ/mol c.-241.8 kJ/mol
表示生成1 mol H2Se的反应热是(填序号);依据是:。
乙醇汽油含氧量达35%,使燃料燃烧更加充分,使用车用乙醇汽油,尾气排放的CO和碳氢化合物平均减少30%以上,有效的降低和减少了有害的尾气排放。但是汽车使用乙醇汽油并不能减少NOx的排放,对NOx的有效消除成为环保领域的重要课题。NOx排入空气中,形成酸雨,造成空气污染。NOx中有一种红棕色气体,其溶于水的方程式是。
(2)已知NO2和N2O4的结构式分别是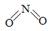 和
和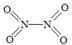 。
。
| 物质 |
NO2 |
N2O4 |
|
| 化学键 |
N=O |
N—N |
N=O |
| 键能(kJ/mol) |
466 |
167 |
438 |
写出NO2转化N2O4的热化学方程式。
(3)研究人员在汽车尾气系统中装置催化转化剂,可有效降低NOx的排放。
① 写出用CO还原NO生成N2的化学方程式。
② 在实验室中模仿此反应,在一定条件下的密闭容器中,测得NO转化为N2的转化率随温度变化情况和n (NO)/n(CO)比例变化情况如下图。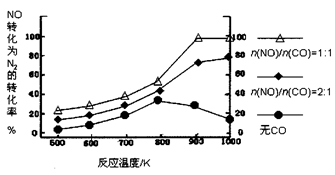
为达到NO转化为N2的最佳转化率,应该选用的温度和n(NO)/n(CO)比例分别为、;该反应的∆H0(填“>”、“<”或“=”)。
(4)用 CxHy(烃)催化还原NOx也可消除氮氧化物生成无污染的物质。CH4与NO发生反应的化学方程式为。