选修:物质结构与性质】(铁和铜都是日常生活中常见的金属,有着广泛的用途。请回答下列问题:
(1)铁在元素周期表中的位置 ______
(2)k3[Fe(CN)6]溶液可用于检验 ______(填离子符号)CN-中碳原子杂化轨道类型为 ____,C、N、O三元素的第一电离能由大到小的顺序为 ___(用元素符号表示)。
(3)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于____________(填晶体类型)。Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=____________。Fe(CO)x在一定条件下发生反应:Fe(CO)x(s)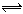 Fe(s)+xCO(g)。已知反应过程中只断裂配位键,则该反应生成物含有的化学键类型有 _________。
Fe(s)+xCO(g)。已知反应过程中只断裂配位键,则该反应生成物含有的化学键类型有 _________。
(4)铜晶体铜碳原子的堆积方式如右图所示。

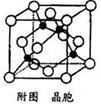
①基态铜原子的核外电子排布式为 ________________。
②每个铜原子周围距离最近的铜原子数目 。
(5)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如附图所示(黑点代表铜原子)。
①该晶体的化学式为 。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于 _______(填“离子”、“共价”)化合物。
③已知该晶体的密度为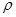 g.cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为 ________________pm(只写计算式)。
g.cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为 ________________pm(只写计算式)。
(9分)㈠金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧时生成二氧化碳,反应中放出的热量如图所示:
⑴等量金刚石和石墨完全燃烧__________(填“金刚石”或“石墨”)放出热量更多,写出表示石墨燃烧热的热化学方程式______________________________;
⑵在通常状况下,金刚石和石墨相比________(填“金刚石”或“石墨”)更稳定,写出石墨转化为金刚石的热化学方程式__________________________;
⑶12g石墨在一定量空气中燃烧,生成气体36g,该过程放出的热量。
㈡⑴家用液化气中主要成分之一是丁烷。当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50KJ。试写出丁烷燃烧反应的热化学方程式;
⑵已知含KOH 28.0g稀溶液与足量稀硫酸反应,放出28.65KJ的热量,试写出该反应中和热的热化学方程式。
某化学反应2A(g) B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
B(g)+D(g)在四种不同条件下进行,B、D起始浓度为0。反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验 序号 |
  时间 时间浓度 温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800℃ |
c2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
800℃ |
c3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
| 4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
⑴在实验1,反应在20至30分钟时间内用A表示表示该反应的平均速率为________。
⑵在实验2,A的初始浓度c2=____________mol/L,反应经20分钟就达到平衡,可推测实验2中还隐含的条件是_______________________________。
⑶设实验3的反应速率为v3,实验1的反应速率为v1,则v3_______v1(填“<”、“=”或“>”),且c3_______1.0 mol/L(填“<”、“=”或“>”)。
⑷比较实验4和实验1,可推测该反应是________反应(选填吸热、放热)。理由是___________________________________________________________。
在80℃时,将0.4mol的A气体充入2L已抽空的固定容积的密闭容器中发生反应:A(g) mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
mB(g)隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) c(mol/L) |
0 |
20 |
40 |
60 |
80 |
100 |
| c(A) |
0.20 |
0.14 |
0.10 |
c |
d |
e |
| c(B) |
0.00 |
0.12 |
b |
0.22 |
0.22 |
0.22 |
⑴m=,表中bc(填“<”、“=”或“>”)。
⑵100秒后若将容器的体积缩小至原来一半,平衡时B的浓度____________0.44 mol/L(填“<”、“=”或“>”)。
⑶在80℃时该反应的平衡常数K值为(保留1位小数)。
⑷在其他条件相同时,该反应的K值越大,表明建立平衡时。
①A的转化率越高②B的产量越大
③A与B的浓度之比越大④正反应进行的程度越大
下图表示在密闭容器中反应:2SO2(g)+O2(g) 2SO3(g),△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是;bc过程中改变的条件可能是;若增大压强时,反应速度变化情况画在c-d处。
2SO3(g),△H<0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是;bc过程中改变的条件可能是;若增大压强时,反应速度变化情况画在c-d处。
煤化工中常需研究不同温度下平衡常数、投料比及热值等问题。
已知:CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ |
400 |
500 |
800 |
| 平衡常数K |
9.94 |
9 |
1 |
试回答下列问题
⑴上述正向反应是反应(填“放热”或“吸热”)。
⑵在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有(选填A、B、C、D、E)。
| n(CO) |
n(H2O) |
n(H2) |
n(CO2) |
|
| A |
1 |
5 |
2 |
3 |
| B |
2 |
2 |
1 |
1 |
| C |
3 |
3 |
0 |
0 |
| D |
0.5 |
2 |
1 |
1 |
| E |
3 |
1 |
2 |
1 |
⑶已知在一定温度下:
C(s)+CO2(g) 2CO(g)平衡常数K;
2CO(g)平衡常数K;
C(s)+H2O(g) CO(g)+H2(g)平衡常数K1;
CO(g)+H2(g)平衡常数K1;
CO(g)+H2O(g) H2(g)+CO2(g)平衡常数K2;
H2(g)+CO2(g)平衡常数K2;
则K、K1、K2之间的关系是K=。
⑷若在500℃时进行,设起始时CO和H2O的起始浓度均为0.010mol/L,在该条件下,CO的平衡转化率为:。
⑸若反应在800℃进行,设起始时CO(g)和H2O(g)共为1mol,水蒸气的体积分数为x;平衡时CO转化率为y,则y随x变化的函数关系式为:y=。