室温时,向20 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生,且混合溶液的体积可看成混合前两溶液的体积之和),下列说法不正确的是: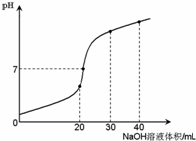
| A.pH=7时,溶液中c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) |
| B.当V(NaOH)=20mL时,溶液中水的电离程度比纯水大 |
| C.当V(NaOH)=30mL时,溶液中 c(SO42-)+ c(H+)= c(NH3·H2O) + c(OH-) |
| D.滴加NaOH溶液从30mL至40mL,溶液中Na+与SO42-浓度之和始终为0.1 mol·L-1 |
原子数相同、电子总数相同的粒子,互称为等电子体。硼元素可形成三个等电子体阴离子:BO2-、BC25-和BN2n-,则BN2n-中的n值为
| A.1 | B.2 | C.3 | D.4 |
下列判断或实验预期正确的是
| A.对于反应N2H4(l)=N2(g)+2H2(g) △H=-50.6kJ·mol-1,它在任何温度下都是自发的 |
| B.用升华法分离碘和氯化铵的混合物,用乙醇萃取碘水中的碘 |
| C.纯碱溶液或石灰水存放在配有磨口塞的棕色玻璃瓶中 |
| D.淀粉用酸催化水解后的溶液加入新制银氨溶液,水浴加热,可看到有银镜出现 |
天然油脂结构的核心为甘油[HOCH2CH(OH)CH2OH],有一瘦身用的非天然油脂,其结构的核心则为蔗糖(C12H22O11),该非天然油脂可由直链型的不饱和油酸(C17H33COOH)与蔗糖反应而得,其反应示意图如图(注:图的反应式不完整)则下列说法不正确的是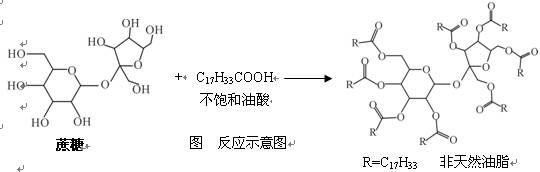
| A.该非天然油脂含有碳碳双键、酯基等官能团。 |
| B.油酸与蔗糖的反应属于皂化反应 |
| C.该非天然油脂与氢氧化钠溶液共热,水解后的产物,可与溴的四氯化碳溶液反应 |
D.蔗糖分子结构中不含醛基,是非还原性糖,不能直接与银氨溶液发 生银镜反应 生银镜反应 |
下列反应的离子方程式正确的是
A.硫化钠的水解反应:S2-+H3O+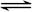 HS-+H2O HS-+H2O |
B.用铜做阳极电解氯化铜溶液:Cu2++2Cl- Cu+Cl2↑ Cu+Cl2↑ |
| C.在硫酸亚铁溶液中通入氧气:4Fe2++O2+4H+=4Fe3++2H2O |
| D.在氢氧化钡溶液中滴加硫酸氢钾溶液至pH=7: |
Ba2++OH-+H++SO42-=BaSO4↓+H2O
生活中处处有化学,下列有关说法正确的是
| A.天然弱碱性水呈碱性的原因是其中含有较多的Mg2+、Ca2+等离子 |
| B.食用地沟油对人体的危害极大,原因主要是里面含有黄曲霉素和甘油三酯 |
| C.地球上CH4、CO2等气体含量上升容易导致温室效应,进而引发灾难性气候 |
| D.保鲜膜、一次性食品袋的主要成分是聚氯乙烯 |