消毒剂在生产生活中有极其重要的作用,开发具有广谱、高效、低毒的杀菌剂和消毒剂是今后发展的趋势。
(1)Cl2、H2O2、ClO2(还原产物为Cl﹣)、O3(1mol O3转化为1mol O2和1mol H2O)等物质常被用作消毒剂.等物质的量的上述物质消毒效率最高的是 (填序号)。
| A.Cl2 | B.H2O2 | C.ClO2 | D.O3 |
(2)H2O2有时可作为矿业废液消毒剂,有“绿色氧化剂”的美称.如消除采矿业胶液中的氰化物(如KCN),经以下反应实现:KCN+H2O+H2O2═A+NH3↑,则生成物A的化学式为 ,H2O2被称为“绿色氧化剂”的理由是 。
(3)漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年.亚氯酸不稳定可分解,反应的离子方程式为HClO2 → ClO2↑+H++Cl﹣+H2O(未配平)。在该反应中,当有1mol ClO2生成时转移的电子个数约为 。
(4)“84”消毒液(主要成分是NaClO)和洁厕剂(主要成分是浓盐酸)不能混用,原因是 (用离子方程式表示)。利用氯碱工业的产物可以生产“84”消毒液,写出有关反应的化学方程式 。
下图的各方框表示有关的一种反应物或生成物(某些物质已经略去),其中常温下A、C、D为无色气体,C能使湿润的红色石蕊试纸变蓝,1molX分解得到A、B、C各1mol。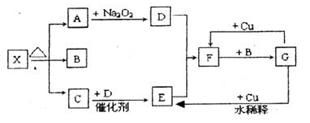
(1)写出下列各物质的化学式:
X:;B:;F:;G:。
(2)写出下列变化的反应方程式:
A→D:;
C→E:。
(3)写出下列变化的离子方程式:
G→E:
G→F:
(4)写出实验室和工业上制C的化学方程式。
A、B、C、D、E、F是中学化学中常见的气体,G是一种固体非金属单质,它们具有如下的性质:
①A、B、E能使湿润的蓝色石蕊试纸变红,F能使湿润的红色石蕊试纸变蓝,C、D不能使湿润的石蕊试纸变色。
②A和F相遇产生白烟。
③B和E都能使品红溶液褪色。
④将红热的铜丝放入装有B的集气瓶中,瓶内充满棕黄色的烟。
⑤C和D相遇生成红棕色气体,且D可助燃。
⑥G是常见的半导体材料
回答下列问题:
(1)A的化学式是,②中的白烟是(填化学式)。
(2)④中发生反应的化学方程式是
(3)C的化学式是,E的化学式是
(4)写出工业上制G的化学方程式
(5)B是一种有毒气体,实验室可用吸收B,反应的离子方程式是
写出实验室制取B的化学方程式
(1)环境专家认为可以用铝将水中的NO3-转化为N2 ,从而清除污染。该反应中涉及的粒子有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将各粒子分别填入以下空格(不用配平)。
NO3- + + → + +
该反应过程中,被氧化与被还原的元素的物质的量之比为。
(2)若4Al(s)+3O2(g) ="2" Al2O3(s)△H=" a" KJ/mol
C(s)+O2(g)=CO2(g)△H=" c" KJ/mol
写出Al与氧化铁发生铝热反应的热化学方程式:。
(3)将一定质量的钠铝合金置于水中,合金全部溶解,得到20mL PH=14的溶液,然后用2mol/L的盐酸滴定,可得到沉淀量与消耗的盐酸体积关系如上图:则反应过程中产生氢气的总体积为L(标准状况)。
如图所示3套实验装置,分别回答下列问题:
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为。
(2)装置2中的石墨是极(填“正”或“负”),该装置发生的总反应的离子方程式为。
(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。取出Cu电极,洗涤、干燥、称量、电极增重 0.64 g。
①电源的M端为极,甲烧杯中铁电极的电极反应为;
②乙烧杯中电解反应的离子方程式为;
③甲、乙两烧杯中生成的气体标准状况下共mL。
在一固定容积为2L的密闭容器内加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生如下反应: N2(g)+3H2(g) 2NH3(g)△H <0
2NH3(g)△H <0
(1)该反应450℃的平衡常数500℃时的平衡常数(填“>”、“<”或“=”);
(2)下列描述中能说明上述反应已达平衡的是
a.3v正(H2)=2v逆(NH3) b.容器中气体的平均相对分子量不随时间而变化
c.容器中气体的密度 不随时间而变化 d.容器中气体的分子总数不随时间而变化
不随时间而变化 d.容器中气体的分子总数不随时间而变化
(3)上述反应若第5分钟时达到平衡,测得NH3的物质的量为0.2mol
计算从反应开始到平衡时,平均反应速率v(N2)为mol/(L·min)
(4)保持其他条件不变,若初始投入量为amolN2、bmolH2、cmolNH3,也可得到与上述相同的平衡,则a、b、c需满足关系式: ;
(5)第5分钟末,保持其它条件不变, 若继续通入0.2 mol的N2和0.6 mol的H2,
则平衡移动(填“向正反应方向”“向逆反应方向”或“不”)。