据环保部门测定,我国一些大城市的酸雨pH=3.5。在酸雨季节铁制品极易腐蚀,则在其腐蚀中正极发生的反应是
| A.Fe-2e-=Fe2+ | B.2H2O+O2+4e-=4OH- |
| C.2H++2e-=H2↑ | D.4OH--4e-=2H2O+O2↑ |
将充有n mL NO和m mL NO2气体的试管倒立于盛水的水槽中,然后通入n mL O2。m>n,则充分反应后,试管中气体在同温同压下的体积为
A.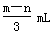 |
B.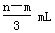 |
C.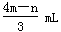 |
D.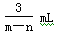 |
往FeCl3和BaCl2的混合溶液中通入SO2,溶液颜色由棕黄色变成浅绿色,同时有白色沉淀产生。下列说法正确的是
| A.该实验表明FeCl3有还原性 | B.白色沉淀为BaSO3 |
| C.该实验表明SO2有漂白性 | D.反应后溶液酸性增强 |
下列原子序数所对应的元素组中,两者可形成离子键的是
| A.1和17 | B.12和9 | C.14和6 | D.15和8 |
下列各组中的每种物质内既有离子键又有共价键的一组是
| A.NaOH、K2SO4、(NH4)2SO4 | B.HCl、Al2O3、MgCl2 |
| C.Na2O2、NH4Cl、Na2SO4 | D.MgO、Na2SO4、NH4HCO3 |
A、B、C为三种短周期元素,A、B同周期,A、C的最低价离子分别为A2-、C-,B2+与C-具有相同的电子层结构,下列叙述不正确的是
| C |
||
| B |
A |
A.离子半径A2->C->B2+
B.它们的原子序数A>B>C
C.它们的原子半径C>B>A
D.原子最外层上的电子数B>A>C