葡萄糖的分子式是___________,
用90g葡萄糖配制成1L水溶液,此溶液的浓度是_______________,
写出葡萄糖在氧气中燃烧的化学方程式_________________________,
90g葡萄糖完全燃烧,生成的CO2气体在标准状况下的体积是____________
(10分)在一定温度下,将2mol A和2mol B两种气体混合于2L密闭容器中,发生反应3A(g)+B(g) 2C(g)+2D(g),2min末反应达到平衡状态,生成0.8 molD。由此推断:
2C(g)+2D(g),2min末反应达到平衡状态,生成0.8 molD。由此推断:
(1)生成D的反应速率。
(2)B的平衡浓度为。
(3)A的转化率为。
(4)该温度下的平衡常数K=。
(5)如果增大反应体系的压强,则平衡体系中C的转化率。(填“增大”或“减小”或“不变”)
某实验小组用0.55 mol/L NaOH溶液和0.50 mol/L盐酸反应来测定中和热,实验装置如下图所示。
(1)图示实验装置中缺少的一种仪器是,大、小烧杯间填满碎纸条的作用是。
(2)氢氧化钠溶液稍过量的原因是。
(3)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会:。(填“偏大”、“偏小”或“无影响”)
(4)实际实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是(填字母)。
a.实验装置保温、隔热效果差
b.用量筒量取盐酸时俯视读数
c.分多次把NaOH溶液倒入盛有盐酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定盐酸的温度
(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,试写出对应的热化学方程式。
标准状况下11.2L氢气在氯气中充分燃烧放出的热量是kJ。
(2)A(g)+B(g) C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
①反应物A(g)和B(g)具有的总能量(填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是__反应(填吸热、放热),△H=(用E1和E2表示)
(每空4分,共12分)
(1)已知:TiO2(s)+2Cl2 (g)===TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)===2CO(g) Δ H=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:。
(2)在25℃,101KPa时,CO的燃烧热为280kJ/mol,写出 CO的燃烧热的热化学方程式:。
(3)在火箭推进器中以肼(N2H4)作为燃料,可以选O2或NO2作为氧化剂,如果以氧气作为氧化剂,其化学反应与能量关系如下,
请写出该反应的热化学方程式
A、B、C是单质,其中A是金属,各种物质间的转化关系如图: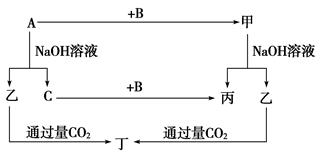
根据图示转化关系回答:
(1)写出下列物质的化学式。
A________________,B________________,乙________________,丁________________。
(2)写出 ①A与NaOH溶液反应的化学方程式_____________________________________________。
②乙溶液中通入过量CO2反应的离子方程式________________________________________。
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为________,有_______mol电子发生转移。