(10分)在一定温度下,将2mol A和2mol B两种气体混合于2L密闭容器中,发生反应3A(g)+B(g) 2C(g)+2D(g),2min末反应达到平衡状态,生成0.8 molD。由此推断:
2C(g)+2D(g),2min末反应达到平衡状态,生成0.8 molD。由此推断:
(1)生成D的反应速率 。
(2)B的平衡浓度为 。
(3)A的转化率为 。
(4)该温度下的平衡常数K= 。
(5)如果增大反应体系的压强,则平衡体系中C的转化率 。(填“增大”或“减小”或“不变”)
对于下列芳香族化合物,命名与结构简式都正确的是( )
(1)主链含5个碳原子,有两个甲基作支链的烷烃有________________种;其中两种
的结构简式是: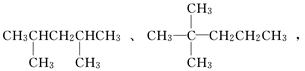 试写出其他几种
试写出其他几种
分子的结构简式,并用系统命名法命名.
________________________________________________________________________
________________________________________________________________________.
(2)以上分子中有一种分子是由烯烃加成得到,而且分子中的碳碳双键只有一种位置,试写出这种烯烃分子的名称________________________________________________.
写出下列物质的结构简式:
(1)2,4,6三甲基辛烷__________________________________________________;
(2)3甲基1丁炔 ____________________________________________________;
(3)间甲乙苯_________________________________________________________;
(4)苯乙烯___________________________________________________________.
某化合物的分子式为C5H11Cl,分析数据表明:分子中含有两个—CH3,两个—CH2—,一个CH和一个 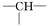 ,写出它可能的结构简式 ______________________
,写出它可能的结构简式 ______________________
已知下列有机物:
①CH3—CH2—CH2—CH3和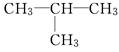
②CH2===CH—CH2—CH3和CH3—CH===CH—CH3
③CH3—CH2—OH和CH3—O—CH3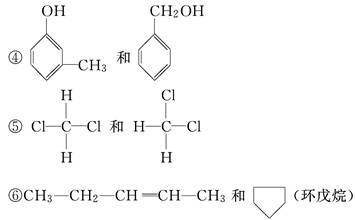
⑦CH2===CH—CH===CH2和CH3—CH2—C≡CH
(1)其中属于同分异构体的是________________.
(2)其中属于碳链异构的是________________.
(3)其中属于位置异构的是________________.
(4)其中属于官能团异构的是________________.
(5)其中属于同一种物质的是________________.