钙元素是人体必须的常量元素,所有细胞都需要钙元素。正常人体血液中钙离子浓度为2.2x10-3mol/L~2.71x10-3mol/L.。请回答下列问题。
(1)血液中钙离子浓度高于或等于2.75x10-3mol/L 称为高血钙症。一个成年人全身血液总量约为4L,则高血钙病人血液中的钙离子至少为 mol;
(2)如果以“g/L”表示,正常人体血液中钙离子浓度的最小值为 g/L;
(3)草酸钙(CaC2O4)难溶于水,是人体内结石的主要成分,其摩尔质量为 g/mol;豆腐中含有较多钙盐(如硫酸钙),硫酸钙的电离方程式是 ;菠菜、洋葱中含有丰富的草酸钠(Na2C2O4),硫酸钙与草酸钠反应的化学方程式是 ,由此说明生活中上述食物正确的食用方法是 。
某烃A 0.2mol在氧气中充分燃烧后,生成化合物B、C各1.2mol。试回答:
(1)烃A的分子式为。
(2)若取一定量的烃A完全燃烧后,生成B、C各3mol,则有g烃A参加了反应,燃烧时消耗标准状况下的氧气L。
(3)若烃A不能使溴水褪色,但在一定条件下,能与氯气发生取代反应,其一氯代物只有一种,则此烃A的结构简式为。
(4)若烃A能使溴水褪色,在催化剂作用下,与氢气加成,其加成产物经测定分子中含有4个甲基。烃A可能有的结构简式为。
如图是常见原电池装置,电流表G发生偏转: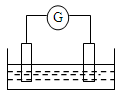
(1)若两个电极分别是Zn、Cu,电解质溶液是稀硫酸,正极的电极反应式为___________________________;如果把电解质溶液换成硫酸铜溶液,则正极的电极反应式为_____________________________。
(2)若总反应是2FeCl3+Fe=3FeCl2,则可以做负极材料的是________,
负极上发生的电极反应是________________________。
(3)若电解质溶液是稀硫酸,Mg、Al两种金属做电极,则Mg电极的电极反应式为_____________;
若电解质溶液换作稀氢氧化钠溶液,Mg、Al两金属做电极,则Mg是____(填“正极”或“负极”),总反应的离子方程式是_______________________________。
针对化学反应中的能量变化解决下列问题。
(1)测定稀硫酸和稀氢氧化钠中和热(中和热为57.3 kJ·mol-1)的实验装置如图所示。某兴趣小组的实验数值结果小于57.3 kJ·mol-1,原因可能是(填字母)。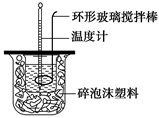
a.实验装置保温、隔热效果差
b.读取混合液的最高温度记为终点温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度
(2)今有如下两个热化学方程式:则ab(填“>”、“=”或“<”)。
H2(g)+1/2O2(g)=H2O(g)ΔH1=a kJ·mol-1
H2(g)+1/2O2(g)=H2O(l)ΔH2=b kJ·mol-1
(3)同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(白磷,s)+5O2(g)=P4O10(s)ΔH=-2983.2 kJ·mol-1①
P(红磷,s)+5/4O2(g)=1/4P4O10(s) ΔH=-738.5 kJ·mol-1②
则白磷转化为红磷的热化学方程式为______________________________。相同状况下,能量状态较低的是_________;白磷的稳定性比红磷_______(填“高”或“低”)。
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2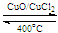 2Cl2+2H2O
2Cl2+2H2O
已知:I.此条件下反应A中,4molHCl被氧化,放出115.6 kJ的热量。
Ⅱ.①写出此条件下,反应A的热化学方程式____________。
②断开1molH-O键与断开1molH-Cl键所需能量相差约为kJ,H2O中H-O键比HCl中HCl键(填“强”或“弱”)。
(10分)为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。试回答下列问题: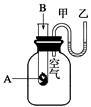
(1)该反应为____________反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量____________(填“高”或“低”)。
(3)物质中的化学能通过化学反应转化成______释放出来。
(4)反应物化学键断裂吸收的能量_______(填“高”或“低”)于生成物化学键形成放出的能量。
(5)写出一个符合题中条件的化学方程式:____________________________。
(13分)U、W、X、Y、Z都是短周期元素,且原子序数依次增大。W的气态氢化物甲和W的最高价氧化物对应的水化物可以化合生成盐,U与X可形成常温下呈液态的分子乙,甲、乙均为常见的10 电子分子;Y元素原子的K层电子数与M层电子数相同;Z元素的单质是太阳能转换为电能的常用材料。请回答问题:
(1)Z元素在周期表中的位置。
(2)X、Y、Z三种元素的原子半径由小到大的顺序是(用元素符号表示)。
(3)U与X形成的18电子化合物的电子式是。
(4)(3)中描述的化合物含有的化学键有。
a.离子键b.极性共价键c.非极性共价键
(5)已知:① N2(g)+3H2(g)=2NH3(g)ΔH=-92.4kJ/mol
②2H2(g)+O2(g)=2H2O(g)ΔH=-483.6kJ/mol
试写出氨气完全燃烧生成气态水和氮气的热化学方程式。
(6)有人设想寻求合适的催化剂和电极材料,以U2、W2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极电极反应式:;溶液中H+移向(填“正”或“负”)极。