针对化学反应中的能量变化解决下列问题。
(1)测定稀硫酸和稀氢氧化钠中和热(中和热为57.3 kJ·mol-1)的实验装置如图所示。某兴趣小组的实验数值结果小于57.3 kJ·mol-1,原因可能是 (填字母)。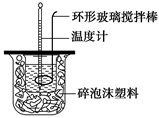
a.实验装置保温、隔热效果差
b.读取混合液的最高温度记为终点温度
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后未洗涤,直接测定H2SO4溶液的温度
(2)今有如下两个热化学方程式:则a b(填“>”、“=”或“<”)。
H2(g)+1/2O2(g)=H2O(g) ΔH1=a kJ·mol-1
H2(g)+1/2O2(g)=H2O(l) ΔH2=b kJ·mol-1
(3)同素异形体相互转化的反应热相当小而且转化速率较慢,有时还很不完全,测定反应热很困难。现在可根据盖斯提出的“不管化学过程是一步完成或分几步完成,这个总过程的热效应是相同的”观点来计算反应热。已知:
P4(白磷,s)+5O2(g)=P4O10(s) ΔH=-2983.2 kJ·mol-1 ①
P(红磷,s)+5/4O2(g)=1/4P4O10(s) ΔH=-738.5 kJ·mol-1 ②
则白磷转化为红磷的热化学方程式为______________________________。相同状况下,能量状态较低的是_________;白磷的稳定性比红磷_______(填“高”或“低”)。
(4)用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2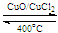 2Cl2+2H2O
2Cl2+2H2O
已知:I.此条件下反应A中,4molHCl被氧化,放出115.6 kJ的热量。
Ⅱ.①写出此条件下,反应A的热化学方程式____________。
②断开1molH-O键与断开1molH-Cl键所需能量相差约为 kJ,H2O中H-O键比HCl中HCl键(填“强”或“弱”) 。
用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出反应的离子方程式。
(1)FeSO4(CuSO4):
所需试剂(填化学式),所涉及的离子方程式:。
(2)O2(CO2):
所需试剂(填化学式),所涉及的离子方程式:。
(1)用标准NaOH溶液滴定未知浓度的盐酸,用酚酞作指示剂,下列操作中会导致实验结果偏低的是。
①碱式滴定管用蒸馏水洗净后没有用标准液润洗
②用酸式滴定管加待测液时,刚用蒸馏水洗净后的滴定管未用待测液润洗
③锥形瓶用蒸馏水洗净后没有用待测液润洗
④滴定前滴定管尖端有气泡,滴定后气泡消失
⑤终点读数时俯视,其他读数方法正确
(2)有一学生在实验室测某溶液的pH。实验时他先用蒸馏水湿润pH试纸,然后用洁净的玻璃棒蘸取试样进行检测。
①该学生的操作(填“正确”或“不正确”),如不正确,请分析是否一定有误差 并说明理由(若正确则此问不用作答)
并说明理由(若正确则此问不用作答)
。
②若按此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是,原因是。
某化学兴趣小组拟用粗氧化铜(含少量铜粉、氧化铁及不溶于酸的杂质)制取
无水氯化铜,其制备步骤如下: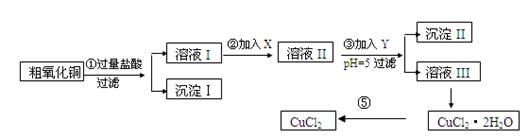
实验过程中所用的物质X,Y及pH控制参照下表确定:
表I
| 物质 |
开始沉淀时pH |
完全沉淀时pH |
| Fe(OH)3 |
2.7 |
3.7 |
| Fe(OH)2 |
7.6 |
9.6 |
| Cu(OH)2 |
5.2 |
6.4 |
表Ⅱ
| 氧化剂 |
调节pH的物质 |
||
| A |
双氧水 |
D |
氨水 |
| B |
高锰酸钾 |
E |
碱式碳酸铜 |
| C |
氯水 |
F |
氧化铜 |
请填写下列空白
(1)沉淀Ⅱ的成分(化学式)是。
(2)步骤②加入的试剂X可选用表Ⅱ中的(填序号),其作用是。
(3)步骤③加入的试剂Y可选用表Ⅱ中的(填序号),控制pH=5的目的是。
(4)步骤⑤要得到无水CuCl2,应控制的条件是。
(5)步骤①中所发生的全部反应的离子方程式:
。
(1)某温度下纯水中c(H+) = 2×10-7 mol/L,则此时水中的C(OH-) =mol/L,若温度不变,向水中滴入稀盐酸使C(H+) = 5×10-6 mol/L,则此时溶液中的c(OH-) = __ mol/L,滴入盐酸后水的离子积(填“变大”“变小”或“不变”,下同),水的电离度。
(2)今有A、 CH3COOH; B、 HCl;C、 H2SO4三种溶液,
①当它们pH相同时,其物质的量浓度关系是(用字母表示, 下同);
下同);
②体积和物质的量浓度相同的三种溶液,分别与同浓度的烧碱溶液反应,要使反应后的溶液呈中性,所需烧碱溶液的体积关系为;
③当它们pH相同、体积相同时,分别加入足量锌,相同状况下产生气体体积关系为。
高炉炼铁过程中发生的主要反应为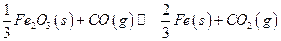
已知该反应在不同温度下的平衡常数如下:
请回答下列问题:
(1)该反应的平衡常数表达式K =_____________,△H______0(填“>”、“<”或“=”);
=_____________,△H______0(填“>”、“<”或“=”);
(2)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过l0 min后达到平衡。求该时间范围内反应的平均反应速率
υ(CO2)= _____________、CO的平衡转化率= ___________;
(3)欲提高(2)中CO的平衡转化率,可采取的措施是__________。
| A.减少Fe的量 | B.增加Fe2O3的量  |
C.移出部分CO2 |
| D.提高反应温度 E.减小容器的容积 F.加入合适的催化剂 |