用NA表示阿佛加德罗常数,下列说法正确的是
| A.标准状况下,2.24L水所含的分子数为0.1 NA |
| B.常温常压下,1.6gO2和O3混合气体中原子总数为0.1 NA |
| C.0.3 mol /L的BaCl2溶液中含Ba2+数目为0.3 NA |
| D.1mol氯气参加氧化还原反应,转移的电子数一定为2 NA |
褪黑素是一种内源性生物钟调节剂,在人体内由食物中的色氨酸转化得到。下列说法不正确的是
| A.色氨酸分子中存在氨基和羧基,可形成内盐,具有较高的熔点 |
| B.褪黑素与色氨酸结构相似,也具有两性化合物的特性 |
| C.在一定条件下,色氨酸可发生缩聚反应 |
| D.在色氨酸水溶液中,可通过调节溶液的pH使其形成晶体析出 |
下列各烷烃进行取代反应后只能生成三种一氯代物的是
A.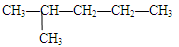 |
B.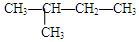 |
C.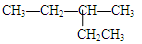 |
D.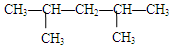 |
下列实验操作能达到实验目的的是
| 选项 |
实验目的 |
实验操作 |
| A |
检验蔗糖水解产物中的葡萄糖 |
取1mL 20%蔗糖溶液,加入少量稀硫酸,水浴加热后取少量溶液于另一试管中,加入几滴新制Cu(OH)2,加热 |
| B |
除去乙烷中混有的少量乙烯 |
将混合气体通入足量酸性KMnO4溶液中 |
| C |
检验葡萄糖中含有醛基 |
向3 mL 2%氨水溶液中加入几滴2%的硝酸银溶液,再加入1mL10%的葡萄糖溶液温水浴加热几分钟 |
| D |
验证蛋白质的盐析 |
向豆浆、鸡蛋清溶液中均滴加饱和硫酸铵溶液,振荡至出现沉淀,再向沉淀物中加入蒸馏水,不断振荡 |
下列化合物,既能发生消去反应,又能发生催化氧化反应的是
| A.CH3OH | B.C2H5OH |
C.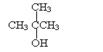 |
D.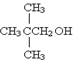 |
下列分子式表示的物质一定是纯净物的是
| A.C2H6O | B.C2H4Cl2 | C.CH4O | D.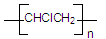 |