用50mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:

(1)从实验装置上看,图中尚缺少的一种玻璃用品是__________.
(2)烧杯间填满碎纸条的作用是__________.
(3)大烧杯上如不盖硬纸板,求得的中和热数值__________(填“偏大、偏小、无影响”)
(4)如果用60mL 0.50mol/L盐酸与50mL 0.55mol/L NaOH溶液进行反应,与上述实验相比,所放出的热量___________________(填“相等、不相等”),所求中和热__________(填“相等、不相等”),简述理由_______ _.
(5)用相同浓度和体积的氨水(NH3•H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会__________;(填“偏大”、“偏小”、“无影响”).
(14分) 如图所示是一个制取Cl2并以Cl2为原料进行特定反应的装置,其中各试剂瓶所装试剂为:B(Na2S)、C(FeBr2)、D(淀粉-KI)、E(SO2和BaCl2)、F(水)、H(紫色石蕊)
(1)写出实验室制取Cl2的化学方程式___________________________________________________________
(2)Ⅰ中b瓶内加入的液体是。装置Ⅰ还可用右图中的装置_______(Ⅱ或Ⅲ)代替
(3)实验开始时,先点燃A处酒精灯,打开分液漏斗旋塞和Ⅰ处活塞,让Cl2充满整个装置,再点燃G处酒精灯,回答下列问题:
①下列装置中的现象是B _________________;D_________________________
②写出E中反应的离子方程式:
_____________________________________;________________________________________
(4)G中硬质玻璃管内盛有碳粉,反应后的产物为CO2和HCl,写出G中的反应的化学方程式__________
(5)在H处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是__________________________
实验室制取乙烯的装置如下图所示,请回答: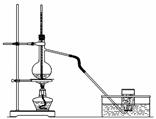
(1)实验室制取乙烯所用的乙醇为无水乙醇,但工业酒精中乙醇的含量为95%,将工业酒精转化为无
水乙醇的方法是。
(2)反应中浓硫酸起和的作用。加热前应该在烧瓶内放入少量碎瓷片,它的作用是。温度计的作用是。
(3)该实验可能产生的主要的有机副产物是。
(4)反应的化学方程式是:反应类型是。
(1)提纯下列物质(括号内为杂质),填写所选用的除杂试剂和除杂方法
| 括号内为杂质 |
除杂试剂 |
操作名称 |
|
| 1 |
乙炔(硫化氢) |
||
| 2 |
溴苯(溴) |
||
| 3 |
苯(苯酚) |
(2)只用一种试剂(可加热)就可区别下列四种无色液体:CH3CH2CH2OH、CH3CH2CHO、HCOOH、CH3COOH,该试剂可以是。
(10分)
某实验需要100 mL、0.1 mol/L的Na2CO3溶液,现通过如下操作配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用(填仪器名称)搅拌
②把①所得溶液冷却到室温后,小心转入(填仪器名称)
③继续加蒸馏水至液面至刻度线1~2cm处,改用(填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切
④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀
⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是(填序号)。
(2)若所配溶液的密度为1.06 g/mL,则该溶液的质量分数为。
(3)若取出20 mL配好Na2CO3的溶液,加蒸馏水稀释成c(Na+) ="0.01" mol/L的溶液,则稀释后溶液的体积为mL
(4)在配制100 mL、0.1 mol/L的Na2CO3溶液时,下列操作中的会导致结果偏低(请用
序号填写)
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.定容时俯视刻度线
c.定容时仰视刻度线
d.干净的容量瓶未经干燥就用于配制溶液
(1)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。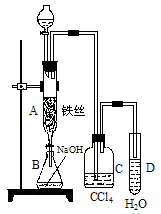
①写出A中有机反应的化学方程式 。
②已知上述有机反应是放热反应,观察到A中的现象是:
及_____ _________。
③ 实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 ,写出有关的化学方程式 。
④C中盛放CCl4的作用是 。
⑤能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中滴入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入______ _____,现象是______________________。
(2)乙炔的实验室制法
①反应原理_____ ____________。
②选择合适的制取实验装置___ ___。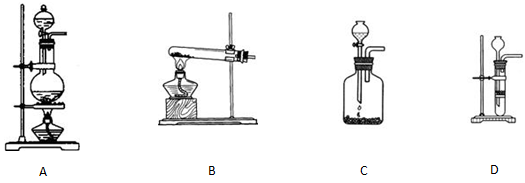
③实验中常用饱和食盐水代替水,目的是______ __________。
④纯净的乙炔气体是无色无味的气体,用电石和水反应制取的乙炔,常含有H2S和PH3而有恶臭气味。可以用____ _______溶液除去杂质气体。