实验室用Na2SO3和70%硫酸溶液反应制取SO2,某研究性学习小组设计如下实验,制取并探究SO2的性质。(制取SO2反应原理为:Na2SO3+2H2SO4=Na2SO4+SO2↑+H2O)
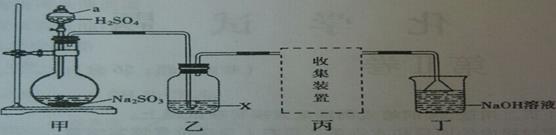
【探究实验】(1)甲装置中a仪器的名称是 。
(2)实验中若生成若生成标准状况下1.12LSO2,则需要Na2SO3 g参加反应。(已知:Na2SO3的摩尔质量为126g·mol-1)
(3)①若X是品红溶液,气体通过乙装置,观察到的现象是 ;
②若X是酸性KMnO4溶液,气体通过乙装置,观察到溶液褪色,说明SO2具有 。
A.酸性 B.还原性 C.漂白性
(4)丁装置中NaOH溶液的作用是吸收多余的SO2,请将其中反应的化学方程式补充完整:
 SO2 +
SO2 + NaOH =
NaOH =  +
+  H2O
H2O
【实验讨论】(5)若X是浓硫酸,用于干燥SO2气体,在丙处选用下图所示的收集装置,
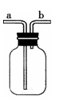
A、B两位同学的连接方式为:
A同学:SO2气体从a导管通入集气瓶中。
B同学:SO2气体从b导管通入集气瓶中。
正确的收集装置是 (填“A”或“B”)同学的连接方式。(已知:同等条件下SO2的密度大于空气)
【知识应用】
(6)向盛有水的烧杯中通入SO2,所得溶液的pH (填“>”或“=”或“<”)7。SO2是形成酸雨的主要物质,请你提出一种减少SO2对空气污染的可行措施: 。
下列实验中,不能达到预期目的的是
①用升华法分离碘和氯化铵的混合物
②用结晶法分离硝酸钾和氯化钠的混合物
③用分液法分离水和硝基苯的混合物
④用蒸馏法分离乙醇(沸点为78.5 ℃)和乙酸乙酯(沸点为77.5 ℃)的混合物
| A.①④ | B.②③ | C.③④ | D.②④ |
某化学兴趣小组为探究SO2的性质,按下图所示装置进行实验。请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是____________________,其中发生反应的化学方程式为_________________________________。
(2)实验过程中,装置B中发生的现象是,说明SO2 具有性;
装置C中发生的现象是,说明 SO2 具有性;
(3)装置D的目的是探究SO2与品红作用的可逆性,请写出实验操作及现象:______________;
(4)尾气可采用溶液吸收。
某学校研究性学习小组开展课题探究:
探究课题Ⅰ.“不同条件对化学反应速率影响的探究”,选用4 mL 0.01 mol·L-1KMnO4溶液与2 mL 0.1 mol·L-1 H2C2O4溶液在稀硫酸中进行实验,改变条件如表:
| 组别 |
草酸的体积(mL) |
温度/℃ |
其他物质 |
| |
2 mL |
20 |
|
| |
2 mL |
20 |
10滴饱和MnSO4溶液 |
| |
2 mL |
30 |
|
| ④ |
1 mL |
20 |
1 mL蒸馏水 |
(1)如果研究催化剂对化学反应速率的影响,使用实验和(用 ①~④表示,下同);如果研究温度对化学反应速率的影响,使用实验和。
(2)对比实验①和④,可以研究对化 学反应速率的影响,实验④中加入1 mL蒸馏水的目的是。
探究课题Ⅱ.该小组查阅资料得知:C2O42-+MnO4-+H+→ CO2↑+Mn2++H2O(未配平),欲利用该反应测定某草酸钠(Na2C2O4)样品中草酸钠的质量分数。该小组称量1.34 g草酸钠样品溶于稀硫酸中,然后用0.200 mol·L-1的酸性高锰酸钾溶液进行滴定(其中的杂质不跟高锰酸钾和稀硫酸反应)。
(1)滴定前是否要滴加指示剂?(填“是”或“否”),请说明理由。
(2)滴定时用(填a或b)滴定管盛装KMnO4标准溶液。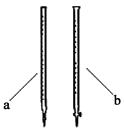
(3)达到终点时消耗了15.00 mL的高锰酸钾溶液,样品中草酸钠的质量分数为。
实验室需要1.0mol/L的NaOH溶液,有如下操作步骤:
①把称量好的4.0gNaOH固体放入小烧杯中,加适量蒸馏水溶解。
②把①所得溶液冷却后小心转入一定容积的容量瓶中。
③继续向容量瓶中加蒸馏水至液面距刻度线1 cm~2 cm处,改用胶头滴管小心滴加蒸馏水至溶液凹液面与刻度线相切。
④用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤的液体都小心转入容量瓶,并轻轻摇匀。
⑤将容量瓶瓶塞塞紧,充分摇匀。
请填写下列空白:
(1)操作步骤的正确顺序为(填序号)。
(2)步骤②所用容量瓶的规格(填序号)
A.100 mL B.250mL C.500 mLD.1000mL
(3)本实验用到的玻璃仪器除容量瓶、玻璃棒外还有______________________________。
(4)需要使用玻璃棒的操作有________(填序号),其作用为。
(5)下列操作会使配得的溶液浓度偏低的是(填序号)
A.容量瓶中原有少量蒸馏水
B.溶液从烧杯转移到容量瓶中后没有洗涤烧杯
C.定容时观察液面俯视
D.配制溶液时,加水超过容量瓶刻度,用胶头滴管将多余溶液吸出
某研究性学习小组利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。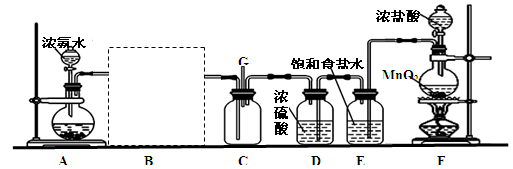
请回答下列问题:
(1)为了快速制备氨气,装置A中烧瓶内的固体可以是(填序号)。
①二氧化硅
②过氧化钠
③生石灰
④氢氧化钠固体
⑤氯化钙
(2)请在B处虚线框内画上合适的装置图并注明所装试剂名称。
(3)装置F中发生反应的离子方程式为:。
(4)装置D和E的位置(填“能”或“不能”)调换,装置E的作用是:。
(5)通入C装置的两根导管左边较长、右边较短,目的是:。
(6)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出发生反应的化学方程式,并标出电子转移的方向和数目:。
(7)从装置C的G处逸出的尾气可能含有污染环境的气体,如何处理?。