化学在可持续发展和能源的综合利用作出了巨大贡献。煤、石油、天然气这些化石能源如何更好的综合利用,相关技术日益成熟,请回答下列问题:
(1)制水煤气的主要化学反应方程式为:C(s)+H2O(g)  CO(g)+H2(g),此反应是吸热反应
CO(g)+H2(g),此反应是吸热反应
①此反应的化学平衡常数表达式为 ;
②下列能增大碳的转化率的措施是 ;(填写相应字母)
| A.加入C(s) | B.加入H2O(g) | C.升高温度 | D.增大压强 |
 (2)合成气合成甲醇的主要反应是:2H2(g)+CO(g) CH3OH(g) △H=-90.8kJ· mol-1
(2)合成气合成甲醇的主要反应是:2H2(g)+CO(g) CH3OH(g) △H=-90.8kJ· mol-1
T℃下此反应的平衡常数为160。此温度下,在2L密闭容器中开始只加入CO、H2,反应10min后测得各组分的物质的量如下:
| 物质 |
H2 |
CO |
CH3OH |
| 物质的量(mol) |
0.4 |
0.2 |
0.8 |
①该时间段内反应速率v(H2)= mol·L-1·min-1。
②比较此时正、逆反应速率的大小:v(正)_______v(逆)(填“>”、“<”或“=”)。
用石油裂化和裂解过程得到的乙烯、丙烯来合成丙烯酸乙酯的路线如下: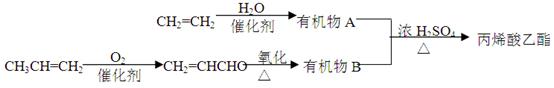
根据以上材料和你所学的化学知识回答下列问题:
(1)丙烯(CH3CH=CH2)中含有的官能团(填名称),A中官能团的电子式__________。
(2)由 CH2=CH2制得有机物A的化学方程式: _______ _,反应类型是 __。
(3)A与B合成丙烯酸乙酯的化学反应方程式是:_____________________________,
反应类型是。
(4)由石油裂解产物乙烯合成聚乙烯塑料的化学方程式是:。
(12分)下述反应中,属于氧化反应的是,属于取代反应的是,属于加成反应的是。
①乙醇在铜催化加热条件下制乙醛的反应
②乙烷在光照条件下与氯气反应
③乙烯使酸性高锰酸钾溶液褪色
④乙烯使溴水褪色
⑤苯与浓硝酸、浓硫酸混合共热制取硝基苯
⑥乙酸和CH3CH218OH在浓硫酸加热条件下生成酯的反应
⑦苯在一定条件下与氢气的反应
写出反应的方程式:①⑤⑥
有一种不饱和醇,其结构简式为CH2=CHCH2OH,请回答下列问题:
(1)写出该化合物中官能团的名称__________。
(2)试推测该化合物可能发生的反应为__________(填序号)。
①与酸性高锰酸钾溶液反应 ②与溴水反应 ③与H2反应
④与Na反应⑤燃烧反应 ⑥催化氧化反应
下列各物质互为同位素的是;互为同素异形体的是;互为同系物的是;互为同分异构体的是_____________;互为同一物质的是
| A.CH2=CH2和CH2=CH—CH=CH2 |
| B.C4H8和C6H12 |
| C.O2和O3 |
D. |
E. 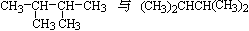
F. C2H6和C4H10G.16O 、18O
H. 金刚石和石墨
I. CH3(CH2)3CH3和(CH3)2CHCH2CH3
J.CH3CH2CH2CH(C2H5)CH3和CH3CH2CH2CH(CH3)C2H5
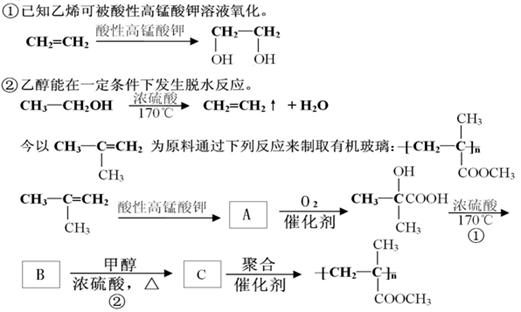
(1)请写出上面方框内的有机物的结构简式
A.B.C.
(2)写出反应①和反应②的化学方程式及反应类型:
反应①:;反应类型
反应②:;反应类型
(3)写出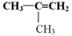 的链状结构的同分异构体中两种物质的结构简式;;
的链状结构的同分异构体中两种物质的结构简式;;