下列说法中正确的是
| A.含有不同种元素的纯净物叫做化合物 |
| B.水溶液中能电离出H+的化合物一定是酸 |
| C.盐中一定含有金属元素 |
| D.含有氧元素的化合物一定是氧化物 |
在下述条件下,一定能大量共存的离子组是
A.无色透明的水溶液中:K+、Ba2+、I-、MnO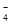 |
B.含有大量NO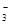 的水溶液中:NH 的水溶液中:NH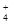 、Fe2+、SO 、Fe2+、SO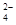 、H+ 、H+ |
C.C(HCO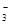 )=0.1 mol·L-1的溶液中:Na+、K+、CO )=0.1 mol·L-1的溶液中:Na+、K+、CO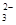 、Br- 、Br- |
D.强碱性溶液中:ClO-、S2-、HSO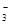 、Na+ 、Na+ |
下列实验设计及其对应的离子方程式均正确的是
| A.用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+= Cu2+ + 2Fe2+ |
| B.Na2O2与H2O反应制备O2:Na2O2 + H2O= 2Na+ + 2OH- + O2↑ |
| C.将氯气溶于水制备次氯酸:Cl2 + H2O= 2H+ + Cl- + ClO- |
D.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+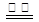 H2↑+ Cl2↑ H2↑+ Cl2↑ |
图表归纳是学习化学的一种常用方法,某同学如下归纳的下表与上图中对应正确的是
| 选项 |
X |
Y |
Z |
 |
| A |
胶体 |
混合物 |
淀粉溶液 |
|
| B |
化合物 |
酸性氧化物 |
一氧化氮 |
|
| C |
气态氢化物 |
化合物 |
液溴 |
|
| D |
强电解质 |
强酸 |
硫酸 |
NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A.1 mol FeI2与足量氯气反应时转移的电子数为2NA |
| B.2 L 0.5 mol·L-1硫酸钾溶液中阴离子所带电荷数为NA |
| C.1 mol Na2O2固体中含离子总数为4NA |
| D.丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA |
在平衡体系:CaCO3(s)  CaO(s) + CO2中仅含有碳酸钙、氧化钙及二氧化碳气体。原压强为P,体积为V,在t0时刻,将容器体积缩小为原来的一半并保持不变。若固体所占体积可忽略,且温度维持不变,则此体系中压强(P 纵坐标)跟时间(t 横坐标)的关系为
CaO(s) + CO2中仅含有碳酸钙、氧化钙及二氧化碳气体。原压强为P,体积为V,在t0时刻,将容器体积缩小为原来的一半并保持不变。若固体所占体积可忽略,且温度维持不变,则此体系中压强(P 纵坐标)跟时间(t 横坐标)的关系为