我国科学家在世界上第一次为一种名为“钴酞菁”的分子(直径为1.3纳米)恢复了磁性,“钴酞菁”分子结构和性质与人体的血红素及植物体内的叶绿素非常相似.下列关于“钴酞菁”分子的说法中正确的是
| A.在水中所形成的分散系属悬浊液 |
| B.分子直径比Na+小 |
| C.在水中形成的分散系能产生丁达尔效应 |
| D.“钴酞菁”分子不能透过滤纸 |
下列物质发生变化时,所克服的粒子间相互作用属于同种类型的是
| A.液溴和苯分别受热变为气体 |
| B.干冰和氯化铵分别受热变为气体 |
| C.二氧化硅和铁分别受热熔化 |
| D.食盐和葡萄糖分别溶解在水中 |
下列叙述正确的是
| A.NH3是极性分子,分子中N原子是在3个H原子所组成的三角形的中心 |
| B.CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心 |
| C.H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央 |
| D.CO2是非极性分子,分子中C原子不处在2个O原子所连成的直线的中央 |
下列说法正确的是
| A.用乙醇或CCl4可提取碘水中的碘单质 |
| B.NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同 |
| C.24Mg32S晶体中电子总数与中子总数之比为1∶1 |
| D.H2S和SiF4分子中各原子最外层都满足8电子结构 |
下列关于晶体的说法一定正确的是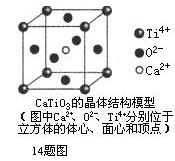
| A.分子晶体中都存在共价键 |
| B.CaTiO3晶体中每个Ti4+和12个O2-相紧邻 |
| C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合 |
| D.金属晶体的熔点都比分子晶体的熔点高 |
PH3一种无色剧毒气体,其分子结构和NH3相似,但P-H键键能比N-H键键能低。下列判断错误的是
| A.PH3分子呈三角锥形 |
| B.PH3分子是极性分子 |
| C.PH3沸点低于NH3沸点,因为P-H键键能低 |
| D.PH3分子稳定性低于NH3分子,因为N-H键键能高 |