黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
S(s)+2KNO3(s)+3C(s)===K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol-1
已知:碳的燃烧热ΔH1=a kJ·mol-1 S(s)+2K(s)===K2S(s) ΔH2=b kJ·mol-1
2K(s)+N2(g)+3O2(g)===2KNO3(s) ΔH3=c kJ·mol-1 则x为( )
| A.3a+b-c | B.c-3a-b |
| C.a+b-c | D.c-a-b |
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量(M)关系,判断下列说法正确的是
| A.若M(甲)<M(乙),则气体的压强:甲>乙 |
| B.若M(甲)>M(乙),则气体的摩尔体积:甲<乙 |
| C.若M(甲)>M(乙),则气体体积:甲<乙 |
| D.若M(甲)<M(乙),则分子数:甲<乙 |
用某仪器测量一液体体积时,平视时读数为nml, 仰视时读数为xml, 俯视时读数为yml,若y >n> x,则所用的仪器可能是
| A.容量瓶 | B.酸式滴定管 | C.碱式滴定管 | D.量筒 |
300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1Ba(OH)2溶液300 mL(忽略溶液体积变化),反应后溶液中SO 的物质的量浓度为( )
的物质的量浓度为( )
| A.0.4 mol·L-1 | B.0.3mol·L-1 | C.0.2 mol·L-1 | D.0.1 mol·L-1 |
下列能达到实验目的的是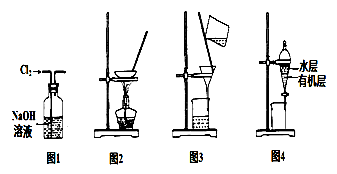
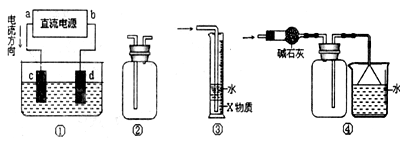
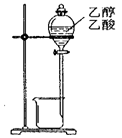
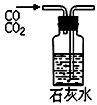
| A.除去Fe(OH)3胶体中的FeCl3 | B.干燥、收集氨气,并吸收多余的氨气 |
| C.分离乙醇、乙酸 | D.除去杂质气体CO2 |
分类是化学研究的重要方法,下列各组物质的分类正确的是( )
| A.同位素:D2、H2、T2 |
| B.含极性键、由分子构成的化合物:CO2、CCl4、NH3 |
| C.非电解质:NH3、C2H5OH、Cl2 |
D.同系物: |