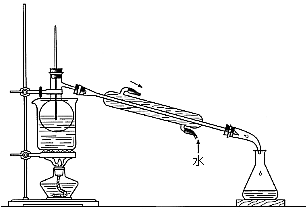
硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
I.[查阅资料]
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水。其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合液中通入SO2可制得Na2S2O3,所得产品中常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
Ⅱ.[制备产品]
实验装置如图所示(省略夹持装置)
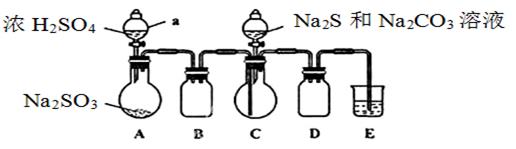
【实验步骤】
①如图示加入试剂。
②先向C中烧瓶加入Na2S和Na2CO3的混合溶液,再向A中烧瓶滴加浓H2SO4。C中发生反应:Na2CO3 + 2Na2S + 4SO2 →3Na2S2O3 + CO2
③待Na2S和Na2CO3完全消耗后,结束反应。C中溶液经一系列的操作可得到Na2S2O3 · 5H2O的粗产品。
(1)仪器a的名称是_________________; E中的试剂可以选用 __ (选填序号)。
a.稀H2SO4 b.NaOH溶液 c.饱和NaHSO3溶液 d.Na2CO3溶液
(2)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案:取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,取沉淀,加入足量稀盐酸, (填实验现象),则可确定产品中含有Na2SO3和Na2SO4。
(3)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤②进行了改进,改进后的操作是 。
Ⅱ.已知:I2+2S2O32-==2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0 mL,恰好反应完全。
(4)根据以上实验和包装袋说明,所测精制盐的碘含量是 mg/kg。(以含w的代数式表示)
实验室里可用甲醇等有关物质制备HCHO,关于甲醇和甲醛的沸点和水溶性见下表:
| 沸点(℃) |
水溶性 |
|
| 甲醇 |
65 ℃ |
与水混溶 |
| 甲醛 |
-21 ℃ |
与水混溶 |
某校化学兴趣小组的甲、乙两位同学,在研究性学习中,运用以上信息和已有知识分别设计了二套实验室制取HCHO装置,如图甲和乙。据此请你回答下列问题: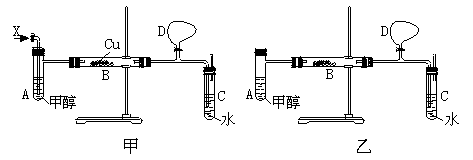
(1)若按甲装置进行实验,则通入A试管的X应是________;B中反应的化学方程式是__________________________________________________。
(2)若按乙装置进行实验,则B管中应装入________。
(3)当实验完成时,若在C中滴加适量银氨溶液,并用水浴将C加热,发生反应的化学方程式是____________________________________________________________。
(4)在反应过程中,甲、乙两种装置中都需直接加热的仪器是________(填A、B、C)
(5)实验开始时,先打开气球D的开关,直至实验结束。气球D的作用是______________________________________________________________________。
(6)从生成甲醛的产量来看,你认为两套装置中较好的是________(填“甲”或“乙”)
某化学兴趣小组的同学对实验室乙酸乙酯的制取和分离进行了实验探究。
【制备】下列是该小组同学设计的实验装置。回答下列问题:
(1)仪器A的名称▲,装置中长导管的主要作用是▲;
(2)证明锥形瓶中收集到乙酸乙酯的简单方法是▲;
【分离】锥形瓶中得到的产物是混合物,为了分离该混合物,设计了如下流程:
(3)a试剂最好选用▲;
(4)操作Ⅰ、操作Ⅱ分别是▲
| A.过滤、分液 | B.萃取、蒸馏 | C.分液、蒸馏 | D.过滤、蒸发 |
【讨论】研究表明质子酸离子液体也可用作酯化反应的催化剂。通过对比实验可以研究不同催化剂的催化效率,实验中除了需控制反应物乙酸、乙醇的用量相同外,还需控制的实验条件是▲。
某同学在学习乙醇的知识后,设计了如下的实验。操作步骤为:
①在试管里加入2 mL 乙醇;
②把一端弯成螺旋状的铜丝放在酒精灯外焰中加热;
③立即将铜丝插入盛有乙醇的试管里(如图),反复操作几次;
④闻生成物的气味,观察铜丝表面的变化。
试回答下列问题:
⑴该实验的目的是;
⑵第④步操作中,能闻到气味;
⑶写出反应的化学方程式。
控制反应条件可改变化学反应速率。
(1)使用催化剂是改变化学反应速率的一种方法,例如H2O2在MnO2作用下分解,请写出该反应的化学方程式:_____________________________。
(2)经研究发现Fe3+和Cu2+对H2O2的分解也具有催化作用。
某研究小组为比较Fe3+和Cu2+对H2O2分解的催化效果,设计了如下实验,请将他们的实验方案补充完整:
实验目的:_________________________________-
实验试剂:5%H2O2溶液,0.1mol/LFeCl3溶液,0.1mol/LCuSO4溶液
实验仪器:试管、胶头滴管
实验步骤:取两支试管各加入1mL5%H2O2溶液,分别滴加两滴0.1mol/LFeCl3溶液、0.1mol/LCuSO4溶液。
该小组的同学可通过观察______________________以比较出Cu2+和Fe3+的催化效果。
问题与讨论:有同学提出将FeCl3改为Fe2(SO4)3更合理,你认为他的理由是____________________________________________________。
(3)影响化学反应速率的因素除催化剂外,还有______________(答出一种即可),并举一例生产、生活实例加以说明:__________________________。
人体必须的元素之一,海洋植物如海带、海藻中含有丰富的、以碘离子形式存在的碘元素。在实验室中,从海藻里提 取碘的流程和实验装置如下:
取碘的流程和实验装置如下: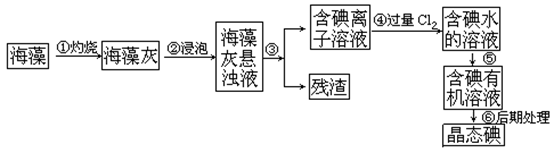
(1)指出上述提取碘的过程中有关实验操作的名称:步骤③______,步骤⑤______。
(2)写出步骤④对应反应的离子方程式:______________________________。
(3)提取碘的过程中,可供选择的有机试剂是_______________。
| A.酒精 | B.醋酸 | C.四氯化碳 | D.苯 |
(4)为了使海藻灰中的碘离子转化为碘的有机溶液,即完成步骤③至⑤,实验室里有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网、以及必要的夹持仪器和物品,尚缺少的玻璃仪器是_________________________________________________________。
(5)从含碘的有机溶剂中提取碘和回收有机溶剂,还需要经过蒸馏。指出下图实验装置中存在的错误之处: 。
。