短周期元素A、B、C、D在周期表中的位置如图所示:B、D最外层电子数之和为12。回答下列问题:

(1)与元素B、D处于同一主族的第2-5周期元素单质分别与H2反应生成1 mol气态氢化物对应的热量变化如下,其中能表示该主族第4周期元素的单质生成1 mol气态氢化物所对应的热量变化是_______(选填字母编号)。
a.吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8 kJ
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2。

①查得:
| 化学键 |
H-H |
Br-Br |
H-Br |
| 键能(kJ/mol) |
436 |
194 |
362 |
试写出通常条件下电解槽中发生总反应的热化学方程式: 。
②根据资料:
| 化学式 |
Ag2SO4 |
AgBr |
| 溶解度(g) |
0.796 |
8.4×10-6 |
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到 ,证明分离效果较好。
③在原电池中,负极发生的反应式为 。
④在电解过程中,电解槽阴极附近溶液pH (填“变大”、“变小”或“不变”)。
⑤将该工艺流程用总反应的化学方程式表示为: 。该生产工艺的优点有 (答一点即可)。
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入________,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为________________ 。
乙烷和丙烷的混合气体完全燃烧后,产物依次通过足量的浓硫酸和过氧化钠,它们分别增重2.04g和2.24g。则乙烷和丙烷的体积比是__________。
有下列各组物质,请按要求填入序号:
A.O2和O3(臭氧)
B.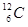 和
和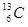
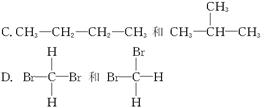
E.甲烷和庚烷
①____________组两物质互为同位素。
②____________组两物质互为同素异形体。
③____________组两物质属于同系物。
④____________组两物质互为同分异构体。
⑤____________组中的物质是同一物质。
相对分子质量为72的烷烃,其分子式是________。若此有机物的一氯代物分子中有两个—CH3,两个—CH2—,一个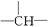 和一个—Cl,它的可能结构分别是________、____________、____________、____________。
和一个—Cl,它的可能结构分别是________、____________、____________、____________。
T℃时,将3mol气体A和1mo1气体B通入容积为2L且固定不变的密闭容器中,发生如下反应:3A(g)+B(g) 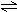 xC(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
xC(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
(1)从反应开始到平衡状态,生成C的平均速率为;X=;
(2)若向原平衡混合物的容器中再充入amolC,在T℃达到新的平衡,此时B的物质的量为n(B)=;
(3)保持温度和容积不变,对原平衡混合物中三者的物质的量作如下调整,可使平衡
向右移动的是;
A.均减半 B.均加倍 C.均增加0.4mol D.均减少0.4mol
(4)若上述可逆反应的热化学方程式为:
3A(g)+B(g) 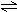 xC(g) ;△H =-QKJ/mol (Q>0)
xC(g) ;△H =-QKJ/mol (Q>0)
①若可逆反应达到平衡后升高体系温度,正反应速率(填“增大”、“减小”或“不变”),平衡将(填“左移”、“右移”或“不移动”)
②若可逆反应达到平衡后增大压强,则体系温度将(填“升高”、“降低”或“不变”)
③若可逆反应达到平衡后,加入A,则△H(填“变大”、“变小”或“不变”
已知具有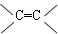 结构的有机物可被酸性高锰酸钾溶液氧化成二元醇,如:CH2=CH2
结构的有机物可被酸性高锰酸钾溶液氧化成二元醇,如:CH2=CH2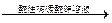 HOCH2CH2OH,现以M(
HOCH2CH2OH,现以M( )为原料合成环状化合物F和高分子化合物E和G。
)为原料合成环状化合物F和高分子化合物E和G。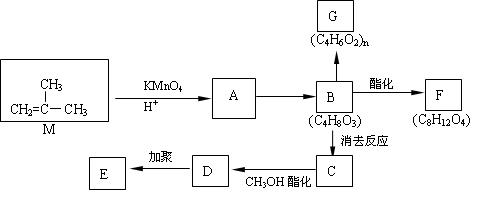
(1)有机物M的名称为;C中的官能团名称是;
A→B的反应类型是。
(2)①B→C的化学方程式。
②B→F的化学方程式。
③两分子B之间发生酯化反应除生成酯F外,还可能生成另外一种酯,该酯的结构简式为。
④D→E的化学方程式。
(3)分子式为C9H10O2的芳香族化合物,属于酯类且只有一个侧连的同分异构体有
种,请写出任意两种的结构简式。