下列溶液中的离子一定能大量共存的是
| A.在加入铝粉能产生氢气的溶液中:NH4+、Fe2+、SO42-、NO3- |
| B.室温下由水电离出的氢离子浓度c(H+)=1×10-14mol/L的溶液中:Ba2+、NO3-、K+、ClO- |
| C.能使酚酞变红色的溶液中:Na+、K+、AlO2-、CO32- |
| D.含大量Fe3+的溶液中:NH4+、Na+、C1-、SCN- |
铜粉放入稀硫酸溶液中,加热后无明显现象发生。当加入一种盐后,铜粉的质量减少,溶液呈蓝色,同时有气体逸出。该盐是 ( )
| A.Fe2(SO4)3 | B.Na2CO3 | C.KNO3 | D.FeSO4 |
如图为周期表中短周期的一部分,若X原子最外层电子数比次外层电子数少3,则下列说法正确的是( )
| R |
||
| X |
Y |
Z |
A、X的氢化物比R的氢化物稳定
B、原子半径大小顺序是Z>Y>X>R
C、Z的单质能与Y的某些化合物发生置换反应
D、X、Y、Z氢化物的稳定性:XH3>H2Y>HZ
以下各种尾气吸收装置中,适合于吸收易溶性气体,而且能防止倒吸的是()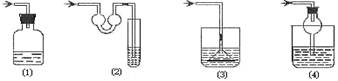
| A.⑴⑵ | B.⑵⑶ | C.⑶⑷ | D.⑵⑷ |
下述实验能达到预期目的的是 ( )
| 编号 |
实验内容 |
实验目的 |
| A |
将SO2通入酸性KMnO4溶液中,使其褪色。 |
证明SO2具有漂白性 |
| B |
将Cl2通入NaBr溶液中 |
比较Cl2与Br2的氧化性强弱 |
| C |
除去CO2中混有少量的CO,点燃燃烧 |
除去CO杂质 |
| D |
盐酸与Na2CO3反应生成CO2 |
证明非金属性:Cl > C |
A、B、C均为短周期元素,A、B同周期,A、C的最低价阴离子分别为A2-、C-,A2-离子半径大于C-,B2+与C-具有相同的电子层结构。下列叙述中一定不正确的是()
A、它们的原子序数A>B>C B 、它们的原子半径C>B>A
C、它们的离子半径A2->C->B2+ D、它们的最外层电子数C>A>B