设NA代表阿伏伽德罗常数的数值,下列说法正确的是( )
| A.1mol硫酸铝钾中阴离子所带电荷数为2NA |
| B.标准状况下,NA个SO3分子所占的体积约为22.4L |
| C.将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NAFe3+ |
| D.标准状况下,22.4L Cl2与足量氢氧化钠溶液反应转移的电子数为NA |
下列实验操作能够达到实验目的的是()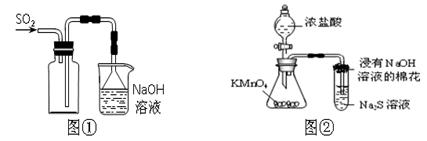
| A.实验室采用图①所示装置收集SO2 |
| B.可用图②所示装置比较KMnO4、Cl2、S的氧化性强弱 |
| C.实验室制取的溴乙烷中常含有少量溴,加适量的苯,振荡、静置后分液,可除去溴乙烷中的溴 |
| D.称取0.40 g NaOH,置于100 mL容量瓶中加水至刻度线,可配制0.10 mol/L NaOH溶液 |
通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一。对下列反应的推断或解释正确的是()
| 操作 |
可能的实验现象 |
解释 |
|
| A |
某溶液中加入硝酸酸化的氯化钡溶液 |
有白色沉淀生成 |
溶液中一定含有SO42- |
| B |
向淀粉KI溶液中不断通入C12 |
溶液变蓝后褪色 |
C12先表现氧化性后表现漂白性 |
| C |
CO还原Fe2O3得到的黑色固体加入盐酸溶解后再加入KSCN溶液 |
溶液不显红色 |
黑色固体没有Fe3O4 |
| D |
将SO2通入BaCl2溶液中 |
没有白色沉淀生成 |
BaSO3可溶于酸 |
下列离子方程式表示正确的是()
| A.AgNO3溶液中加入Cu:Cu + Ag+ = Cu2+ + Ag |
| B.FeCl2溶液中滴加NaClO溶液生成红褐色沉淀:2Fe2+ + ClO- + 5H2O= 2Fe(OH)3↓+Cl-+ 4H+ |
| C.甲酸溶液滴到大理石台板上有气泡产生:2H+ + CaCO3 = CO2↑+ Ca2+ + H2O |
| D.等体积等物质的量浓度的NaHCO3和Ba(OH)2溶液混合:HCO3- + Ba2+ + OH- = BaCO3↓+ H2O |
已知氯气、溴蒸气分别跟氢气反应的热化学方程式如下(Q 1、Q2均为正值):
H2(g)+Cl2(g) = 2HCl(g) △H1=-Q1 kJ·mol-1
H2(g)+Br2(g) = 2HBr(g) △H2=-Q2 kJ·mol-1
有关上述反应的叙述正确的是( )
| A.Q1< Q2 |
| B.生成物总能量均高于反应物总能量 |
| C.1 mol HBr(g)具有的能量高于1 mol HBr(l)具有的能量 |
| D.生成1 mol HCl气体时放出Q1热量 |
A、B、C和D都是周期表中前20号元素,已知A的阳离子和C的阴离子具有相同的核外电子排布,且能形成组成为AC的化合物;C和D属同族元素,其中C中核外电子数是D中核内质子数的2倍。B和D同周期且B的同素异形体之一是原子晶体。下列说法中正确的是()
A.D元素处于元素周期表中第2周期第Ⅵ族
B.AD2中可能既有离子键又有共价键
C.四种元素的原子半径A>C>D>B
D.BCD分子一定是直线型非极性分子