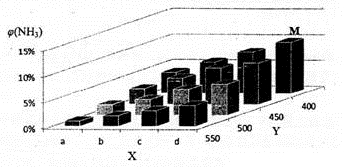
1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才。现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产:N2(g)+3H2(g) 2NH3(g)△H<0。当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如下图所示。
2NH3(g)△H<0。当改变某一外界条件(温度或压强)时,NH3的体积分数ψ(NH3)变化趋势如下图所示。
回答下列问题:
(1)已知: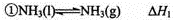 ,
, ,则反应N2(g)+3H2(g)
,则反应N2(g)+3H2(g) 2NH3(g)的△H= (用含△H1、△H2的代数式表示)。
2NH3(g)的△H= (用含△H1、△H2的代数式表示)。
(2)合成氢的平衡常数表达式为____ ,平衡时,M点NH3的体积分数为10%,则N2的转化率为____ (保留两位有效数字)。
(3)X轴上a点的数值比b点 (填“大”或“小”)。上图中,Y轴表示 (填“温度”或“压强”),判断的理由是 。
(4)若将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件和平衡时的相关数据如下表所示:
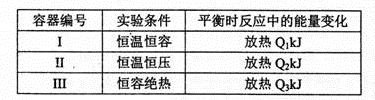
下列判断正确的是_____________。
| A.放出热量:Ql< Q2< △Hl | B.N2的转化率:I> III |
| C.平衡常数:II >I | D.达平衡时氨气的体积分数:I>II |
(5)常温下,向VmL amoI.L-l的稀硫酸溶液中滴加等体积bmol.L-l的氨水,恰好使混合溶液呈中性,此时溶液中c(NH4+)______________c(SO42-)(填“>”、“<”或“=”)。
(6)利用氨气设计一种环保燃料电池,一极通入空气,另一极通入氧气,电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,它在熔融状态下能传导O2-。写出负极的电极反应式_ _________。
I.常温下浓度均为0.l mol/L的下列溶液:①Na2CO3溶液②NaHCO3溶液③盐酸④氨水
回答下列问题。
(1)上述溶液中有水解反应发生的是(填编号,下同),溶液中溶质存在电离平衡的是。
(2)四种溶液中对水的电离抑制作用最大的是;比较①、②溶液,pH较大的是。
(3)在溶液④中加入NH4Cl固体,NH+4浓度与OH-浓度的比值将____(填“变大”、“变小”、“不变”)
II.有一瓶无色澄清溶渡,其中可能含有:NH+4、K+、Mg2+、Al3+、Fe2+、NO-3、Cl-、SO2-4、CO2-3取该溶液进行下列实验:
(1)取部分溶液,向其中逐滴滇入Ba(OH
 )2溶液至过量,有白色沉淀生成,沉淀量与加入Ba(OH)2溶液量的关系如右图所示。
)2溶液至过量,有白色沉淀生成,沉淀量与加入Ba(OH)2溶液量的关系如右图所示。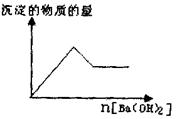
(2)取(I)反应后过滤所得沉淀和滤液,在沉淀中加入稀盐酸后,沉淀不减少。将滤液分为两等份,一份加热,未产生刺激性气味的气体;另一份如HNO3酸化时有白色沉淀产生,继续加HNO3,沉淀又消失,再加AgNO3没有变化。
根据以上事实确定:该溶液中肯定 存在的离子有;
存在的离子有;
肯定不存在的离子有____。
I.(1)亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
Na2SO3+KIO3+H2SO4——Na2SO4+K2SO4+ I2+H2O
①配平上面的氧化还原反应方程式,将计量数填在方框内。
②其中氧化剂是,若反应中有5 mol电子转移,则生成的碘是mol。
(2)0.3 mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ热量,乙硼烷燃烧热的热化学方程式为。
II.含氰化物(有CN-)的废水危害大,CN-的含量为0.01mol/L~0.04mol/L就能毒 杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。
杀鱼类。其处理方法是用氧化法使其转化为低毒的氰酸钾(KCNO),氧化剂常用次氯酸盐;而生成的CNO-可进一步降解为能直接排放到空气中的无毒气体。近期研究将把某些导体的小粒悬浮在溶液中,在光的作用下,在小粒和溶液界面发生氧化还原反应。但小粒的质量和性质不发生变化,如二氧化钛(TiO2)小粒表面就可以破坏氰化物等有毒废物。
(1)二氧化钛在上述反应中的作用是。
(2)CNO-经进一步处理后产生的两种无毒气体应该是和。
(3)若用NaClO溶液处理NaCN的废液,产生另外两种盐,其化学方程式为。
短周期元素A、B、C、D、E原子序数依次增大,其中D是日常生活中常见的金属元素,E是所在周期原子半径最小的主族元素,A、B、C分别位于不同周期,且A和C同主族。回答下列问题:
(1)B和A组成的简单化合物与B元素最高价的含氧酸反应生成一种盐,则B和A组成的简单化合物的化学式为,其空间构型为型,属于(填“极性”或“非极性”)分子。
(2)D原子结构示意图为,C的晟高价氧化物对应水化物与D的最高价氧化物 对应水化物反
对应水化物反 应的离子方程式为。
应的离子方程式为。
(3)在B和A组成的简单化台物与BE3这两种物质中B元素的化合价相同,其中BE3 可与水发生水解反应,其中会生成一种强氧化性物质,则反应方程式为,该强氧化性物质的结构式为。
可与水发生水解反应,其中会生成一种强氧化性物质,则反应方程式为,该强氧化性物质的结构式为。
(1 6分)某芳香族化合物A的分子中含有C.H、O、N四种元素,相同状况下,其蒸气的密度为氢气密度的68.5倍。现以苯为原料合成A,并最终制得F(一种染料中间体),转化关系如下(一些非主要产物己略去):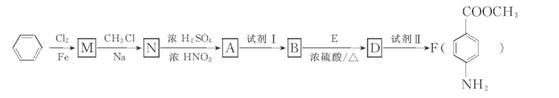
己知: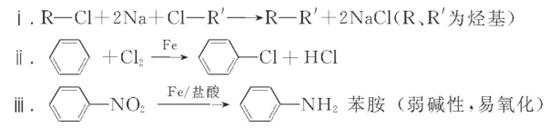
请回答下列问题:
(1)写出 A的结构简式。
(2)N→A的反应类型是。
(3)①上述转化中试剂I和试剂Ⅱ分别是:试剂I;试剂Ⅱ(选填字母)。
a. KMnO4(H+) b.Fe/盐酸 c.NaOH溶液
②若上述转化中物质A依次与试剂Ⅱ、试剂I、化合物E(浓硫酸j△)作用,能否得到F?,为什么? 。
(4)用核磁共振氢谱可以证明化合物E中含有种处于不同化学环境的氢。
(5)写出同时符合下列要求的两种D的同分异构体的结构简式:
①属于芳香族化合物,分子中有两个互为对位的取代基,其中一个取代基是硝基;
②分子中含有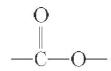 结构。
结构。
(6)有一种D的同分异构体w,在酸性条件下水解后,可得到一种能与FeCl3溶液发生显色反应的产物,写出w在酸性条件下水解的化学方程式:。
(7)F的水解反应如下: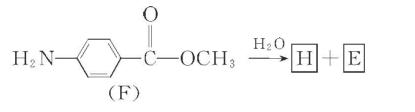
化合物H在一定条件下经缩聚反应可制得高分子纤维,广泛用于通讯、导弹、宇航等领域。请写出该缩聚反应的化学方程式:
有关元素X、Y、Z、W的信息如下:
| 元素 |
信息 |
| X |
所在主族序数与所在周期序数之差为4 |
| Y |
最高价氧化物对应的水化物,能电离出电子数相等的阴、阳离子 |
| Z |
单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏 |
| W |
基态原子核外5个能级上有电子,且最后的能级上只有1个电子 |
请回答下列问题:
(1)W的单质与Y的最高价氧化物对应的水化物反应的离子方程式为
(2)铜片、碳棒和ZX3溶液组成原电池,写出正极发生的电极反应方程式
(3)向淀粉碘化钾溶液中滴加几滴ZX3的浓溶液,现象为,Z3+离子的电子排布式为,它有个未成对电子。
(4)以上述所得WX3溶液为原料制取无水WX3,先制得WX3·6H2O晶体,主要操作包括,在条件下加热WX3·6H2O晶体,能进一步制取无水WX3,其原因是(结合离子方程式简要说明)。