在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g) nY(g)ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g)ΔH=Q kJ·mol-1。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
下列说法正确的是
| A.m>n |
| B.温度不变,压强增大,Y的质量分数减少 |
| C.Q<0 |
| D.体积不变,温度升高,平衡向逆反应方向移动 |
实验室用食盐制纯碱的操作步骤是:
(1)向浓氨水中加入足量食盐晶体制取饱和氨盐水;
(2)向饱和氨盐水中通入足量的二氧化碳气体至有大量晶体析出;
(3)将操作(2)中产生的晶体过滤出来;
(4)将滤纸上的晶体转移至坩埚中,加热至不再有水蒸气产生,所得固体即为碳酸钠。
对上述信息的有关理解中,正确的是(双选)( )
| A.用食盐制纯碱还需要含碳元素的物质 |
| B.食盐水比氨盐水更易吸收二氧化碳 |
| C.室温下碳酸氢钠的溶解度比氯化铵的溶解度小,所以先结晶析出 |
| D.在氨盐水中如果没有未溶解的食盐晶体存在,说明溶液一定不饱和 |
下列叙述中正确的是( )
| A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成 |
| B.向Na2CO3溶液中逐滴加入等物质的量的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2 |
| C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相等 |
| D.向Na2CO2饱和溶液中通入CO2,有结晶析出 |
我国化学家侯德榜根据通常情况下,NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl===NaHCO3↓+NH4Cl等反应原理制取纯碱,实验室也可模拟工业方法制备碳酸钠。下面是模拟实验的示意图:
其中气体A、B分别是CO2和NH3之一。下列有关过程的叙述错误的是( )
A.A气体是CO2,B气体是NH3
B.侯氏制碱法的最终产品是Na2CO3和NH4Cl
C.是在NH3的饱和溶液中加食盐,还是在CO2的饱和溶液中加食盐与两种气体的溶解度及在水中的电离平衡有关
D.第Ⅲ步操作过滤所得的晶体是NaHCO3,第Ⅳ步操作是灼烧
油脂是油与脂肪的总称,它是多种高级脂肪酸的甘油酯。油脂既是重要的食物,又是重要的化工原料。油脂的以下性质和用途与其含有的不饱和双键(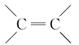 )有关的是( )
)有关的是( )
| A.适量摄入油脂,有助于人体吸收多种脂溶性维生素和胡萝卜素 |
| B.利用油脂在碱性条件下的水解,可以生产甘油和肥皂 |
| C.植物油通过氢化可以制造植物奶油(人造奶油) |
| D.脂肪是有机体组织中储存能量的重要物质 |
下列属于油脂的用途是( )
①人类的营养物质 ②制取肥皂 ③制取甘油 ④制备高级脂肪酸 ⑤制备汽油
| A.①②③ | B.①③⑤ |
| C.②③④⑤ | D.①②③④ |