有下列三个反应:
①Cl2+FeI2=FeCl2+I2;②2Fe2++Br2=2Fe3++2Br-;③CO2O3+6HCl=2COCl2+Cl2↑+3H2O下列说法正确的是
| A.① ② ③中的氧化产物分别是I2、Fe3+、COCl2 |
| B.根据以上方程式可以得到氧化性Cl2>Fe3+>CO2O3 |
| C.可以推理得到Cl2+FeBr2=FeCl2+Br2 |
| D.在③反应中当1mol CO2O3参加反应时,2mol HCl被氧化 |
下列有关化学用语的说法中不正确的是
| A.次氯酸的结构式为:H—Cl—O | B.-OH与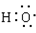 都表示羟基 都表示羟基 |
C.S2-的结构示意图:S2-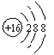 |
D.苯分子的模型示意图: |
下述实验操作能达到预期实验目的的是
| 编号 |
实验操作 |
实验目的 |
| A |
将10g(CuSO4·5H2O溶解在90g水中 |
配制质量分数为10%的CuSO4溶液 |
| B |
向盛有1mL 0.1mol·L-1AgNO3溶液的试管中滴加0.1 mol·L-1NaCl溶液,至不再有沉淀生成,再滴加0.1mol·L-1KI溶液 |
证明一种沉淀能转化为溶度积更小的另一种沉淀 |
| C |
室温下,分别向2支试管中加入相同体积、相同浓度的Na2S2O3溶液,再分别加入相同体积不同浓度的稀硫酸 |
研究温度对化学平衡的影响 |
| D |
甲苯中滴入少量浓溴水,振荡,静置 |
证明甲苯能和溴发生取代反应 |
关于右图所示的原电池,下列说法正确的是
| A.电子从锌电极通过检流计流向铜电极 |
| B.盐桥中的阴离子向硫酸铜溶液中迁移 |
| C.锌电极发生还原反应,铜电极发生氧化反应 |
| D.铜电极上发生的电极反应是2H++e-→H2↑ |
有人认为CH2=CH2与Br2的加成反应,实质是Br2先断裂为Br+和Br-,然后Br+首先与CH2=CH2一端碳原子结合,第二步才是Br-与另一端碳原子结合。根据该观点如果让CH2=CH2与Br2在盛有NaCl和NaI的水溶液中反应,则得到的有机物不可能是
| A.BrCH2CH2Br | B.CICH2CH2CI | C.BrCH2CH2I | D.BrCH2CH2Cl |
某醇R-CH2-CH2-OH分子中化学键如下所示,则下列说法错误的是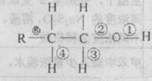
| A.发生催化氧化反应时,被破坏的键是①和③ |
| B.发生消去反应时,被破坏的键是②和④ |
| C.发生酯反应时,被破坏的键是② |
| D.与HX发生取代反应时,被破坏的键② |