滴定实验是化学学科中重要的定量实验。 请回答下列问题:
(1)酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液,下列操作造成测定结果偏高的是______(填选项字母)
A、滴定终点读数时,俯视滴定管刻度,其他操作正确。
B、盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗
C、酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗
D、滴定前,滴定管尖嘴有气泡,滴定后气泡消失
(2)氧化还原滴定——取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol·L-1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
| 滴定次数 |
待测液体积(mL) |
标准KMnO4溶液体积(mL) |
|
| 滴定前读数 |
滴定后读数 |
||
| 第一次 |
25.00 |
0.50 |
20.40 |
| 第二次 |
25.00 |
3.00 |
23.00 |
| 第三次 |
25.00 |
4.00 |
24.10 |
①滴定时,KMnO4溶液应装在 (填“酸”或“碱”)式滴定管中,滴定终点时滴定现象是 。
②该草酸溶液的物质的量浓度为_____________。
(3)沉淀滴定――滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶。参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是 (填选项字母)。
| 难溶物 |
AgCl |
AgBr |
AgCN |
Ag2CrO4 |
AgSCN |
| 颜色 |
白 |
浅黄 |
白 |
砖红 |
白 |
| Ksp |
1.77×10-10 |
5.35×10-13 |
1.21×10-16 |
1.12×10-12 |
1.0×10-12 |
A.NaCl B.NaBr C.NaCN D.Na2CrO4
下图所示是制取无水氯化铜的实验装置图,将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请回答下列问题: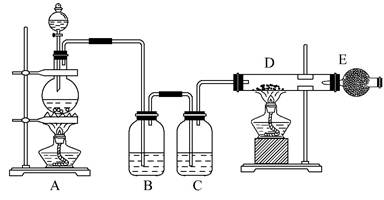
(1)盛放浓盐酸的仪器名称为 。
(2)烧瓶中发生反应的化学方程式为
。
(3)C瓶中的试剂是 ;其作用是
。
(4)玻璃管D中发生反应的化学方程式是
,
反应现象是 。
(5)干燥管E中盛有碱石灰(CaO+NaOH),其作用是
。
某同学帮助水质检测站配制480 mL 0.5 mol·L-1NaOH溶液以备使用。
(1)该同学应选择 mL的容量瓶。
(2)其操作步骤如乙图所示,则甲图操作应在乙图中的 (填选项字母)之间。
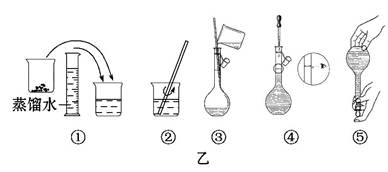
A.②与③ B.①与② C.③与④
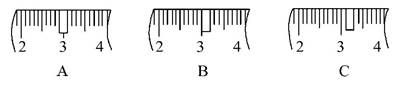
(3)该同学应称取NaOH固体 g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小 (填字母),并在下图中选出能正确表示游码位置的选项 (填字母)。
附表 砝码规格
| a |
b |
c |
d |
e |
|
| 砝码大小/g |
100 |
50 |
20 |
10 |
5 |
用Na2CO3·10H2O晶体,配制0.2 mol·L-1的Na2CO3溶液480 mL。
(1)应称取Na2CO3·10H2O晶体的质量为 。
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体失去了部分结晶水
②碳酸钠晶体不纯,其中混有氯化钠
③称量碳酸钠晶体时所用砝码生锈
④容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有 (填序号,下同),偏低的有 ,无影响的有 。
(3)某同学改用固体Na2CO3配制上述Na2CO3溶液的过程如图所示:
你认为该同学的错误步骤有 (填序号)。
| A.1处 | B.2处 | C.3处 | D.4处 |
甲乙两位同学分别用不同的方法配制100 mL 3.6 mol·L-1的稀硫酸。
(1)若采用18 mol·L-1的浓硫酸配制溶液,需要用到浓硫酸的体积为 。
(2)甲同学:量取浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①将溶液转移到容量瓶中的正确操作是
。
②洗涤操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是 。
③定容的正确操作是 。
(3)乙同学:用100 mL量筒量取浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL刻度线,再搅拌均匀。你认为此法是否正确?若不正确,指出其中错误之处
。
某同学在实验室欲配制物质的量浓度均为1.0 mol/L的NaOH溶液、稀硫酸各450 mL。
提供的试剂是:NaOH固体、98%的浓硫酸(密度为1.84 g/cm3)和蒸馏水。
(1)请你观察图示判断其中不正确的操作有________(填序号)。
(2)应用托盘天平称量NaOH________g,应用量筒量取浓硫酸________mL。
(3)浓硫酸溶于水的正确操作方法是_____________________________。
(4)在配制上述溶液实验中,下列操作引起结果偏低的有________。
A 该学生在量取浓硫酸时,俯视刻度线
B 称量固体NaOH时,将砝码和物品的位置颠倒
C 溶解硫酸后没有冷却至室温就立即完成后面的配制操作
D.在烧杯中溶解搅拌时,溅出少量溶液
E.没有用蒸馏水洗涤烧杯2~3次,并将洗液移入容量瓶中
F.将量筒洗涤2~3次,并全部转移至容量瓶中
G.容量瓶中原来存有少量蒸馏水
H.胶头滴管加水定容时俯视刻度