镍是有机合成的重要催化剂。某化工厂有含镍催化剂废品(主要成分是镍,杂质是铁、铝单质及其化合物,少量难溶性杂质)。某学习小组设计如下流程利用含镍催化剂废品制备硫酸镍晶体:

几种难溶碱开始沉淀和完全沉淀的pH:
| 沉淀物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Ni(OH)2 |
| 开始沉淀 |
3.8 |
2.7 |
7.6 |
7.1 |
| 完全沉淀 |
5.2 |
3.2[来 |
9.7 |
9.2 |
回答下列问题:
(1)溶液①中含有金属的离子是 。
(2)用离子方程式表示加入双氧水的目的 。
(3)操作b调节溶液范围为3.2~7.1,其目的是 ,固体②的化学式为 。
(4)操作a和c需要共同的玻璃仪器是 。上述流程中,防止浓缩结晶过
程中Ni2+水解的措施是 。
(5)如果加入双氧水量不足或“保温时间较短”,对实验结果的影响是 。
设计实验证明产品中是否含“杂质”: 。(不考虑硫酸镍影响)
(6)取2.000 g硫酸镍晶体样品溶于蒸馏水,用0.2000 mol•L-1的EDTA(Na2H2Y)标准溶液滴定至终点,消耗EDTA标准溶液为34.50 mL。反应为Ni2++H2Y2-=NiY2-+2H+。计算样品纯度为 。(已知,NiSO4•7H2O相对分子质量为281,不考虑杂质反应)。
X、Y、Z、W是元素周期表前四周期常见的四种元素,原子序数依次增大。X原子核外有两种形状的电子云,四种伸展方向,常温下以双原子分子存在,性质稳定;Y的单质是生活中常见的合金材料成分之一,原子核外只有一个未成对电子,Z原子的半径比X大,其基态原子最外层的p电子是该层s电子的两倍,W是最常见的黑色金属之一。
(1)Z位于元素周期表中的位置是,W3+的最外层电子排布式是______,X的氧化物XO2与H2O比较,熔点较高的是______ (填化学式)。
(2)加热条件下,Z的单质与足量的X的最高价氧化物的水化物的浓溶液反应,生成Z的最髙价含氧酸,写出此反应的化学方程式。.
(3)比较Y、W性质的活泼性(用一个化学反应方程式表示)。
(4)2013年初,全国各地多个城市都遭遇“十面霾伏”,造成“阴霾天”的主要根源之一是汽车尾气和燃煤尾气排放出来的固体小颗粒PM2.5。汽车尾气净化的主要原理为:2NO(g)+2CO(g)  2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
据此判断:
该反应为反应(放热、吸热);在T2温度下,0~2s内的平均反应速率:υ(N2)=;
(5)当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,
在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
(6)若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是(填代号)。
(下图中υ正、K、n、w分别表示正反应速率、平衡常数、物质的量和质量)
我国从澳大利亚进口的某高炉生铁(用A表示)的成分如下(其余是铁):
| C |
Si |
Mn |
P |
S |
| 4.070% |
2.900% |
0.495% |
0.165% |
0.010% |
(1)称取100.000g A经过一系列处理(最后一步是在空气中灼烧)后,锰全部转变为某种氧化物,其质量为0.687g,则其化学式为。
(2)磷肥的肥效以相当含P2O5多少来表示。炼钢时,P元素形成炉渣Ca3(PO4)2,后者再与浓硫酸反应制得普通过磷酸钙[即普钙,成分是CaSO4、Ca(H2PO4)2和少量其它杂质]。若某普钙中Ca(H2PO4)2的质量分数为45.25%,则含P2O5的质量分数至少是%。
(3)锰的质量分数为30%的高锰钢有很好的性能,可制作火车车轮。将A冶炼成含碳0.4%、含锰30%的高锰钢(设铁无损耗,其它杂质已除去,可补充锰),则100吨A可制得高锰钢吨。
(4)某炼钢厂的烟尘成分和质量分数如下表:
| FeO |
Fe2O3 |
CaO |
|
| 烟尘煅烧前(%) |
86.40 |
4.00 |
9.60 |
为了减少烟尘的排放,将烟尘与CO混合后在空气中煅烧,得到铁的氧化物和CaO的烧结物,其中CaO的质量分数为8.92%(金属元素无损耗),烧结物分离出CaO后,若铁的氧化物中只有两种物质组成,则铁的氧化物的组成和物质的量之比如何?
某芳香烃X(相对分子质量为92)是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为(C7H5NO)。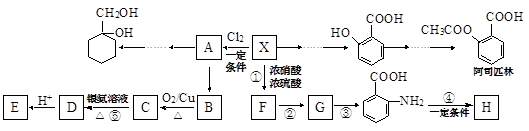
已知: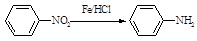 (苯胺,易被氧化)
(苯胺,易被氧化)
完成下列填空:
(1)X的结构简式是,反应⑤的类型是。
(2)反应②③两步能否互换(填“能”或“不能”),理由是。
(3)反应④的化学方程式是。
(4)检验B是否完全转化为C的方法是(选填编号)。
a.定量分析:测熔点 b.定性分析:酸性高锰酸钾溶液
c.定量分析:银氨溶液 d.定性分析:新制氢氧化铜
A为某有机合成的中间体,分子内无支链,在一定条件下发生消去反应可能得到两种互为同分异构体的产物,B是其中的一种,可用于制取合成树脂、染料等多种化工产品。A能发生如下图所示的变化。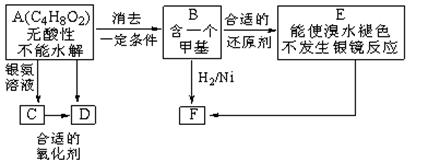
已知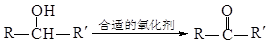 (注:R、R´为烃基)
(注:R、R´为烃基)
试回答:
(1)在A的同分异构体中
a.写出一种具有酸性的结构简式____________________,
b.能发生水解反应的有____________种。
(2) C→D的反应类型是___________,E→F的反应类型是___________。
a.氧化反应 b.还原反应 c.加成反应 d.取代反应
(3) D的结构简式是_____________。
(4)写出E生成高聚物的化学方程式:______________。
(5)两分子C脱去两分子水形成含有八元环的M,写出M的结构简式:________________________。
一定温度下,在2L密闭容器中NO2和O2可发生下列反应: 4NO2(g)+O2(g)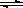 2N2O5(g)+5286 kJ已知体系中n(NO2)随时间变化如下表:
2N2O5(g)+5286 kJ已知体系中n(NO2)随时间变化如下表:
| t(s) |
0 |
500 |
1000 |
1500 |
| n(NO2)(mol) |
20 |
13.96 |
10.08 |
10.08 |
(1)能说明该反应已达到平衡状态的是。
A.v(NO2)=4v(O2) B.容器内压强保持不变
C.v逆(N2O5)=2v正(O2) D.容器内密度保持不变
(2)反应达到平衡后,NO2的转化率为,此 时若再通入一定量氮气,则NO2的转化率将(填“增大”、“减小”、“不变”)。
(3)图中能表示N2O5的浓度变化的曲线是,用O2表示从0~500s内该反应的平均速率v=。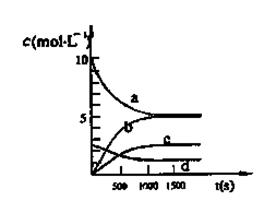
(4)能使该反应的反应速率增大,且平衡向正应方向移动的是。
A.及时分离出NO2气体 B.适当升高温度
C.增大O2的浓度D.选择高效催化剂