铬是不锈钢中一种重要的元素,铬的毒性与其存在的价态有关,低价铬对人体基本无害,六价铬比三价铬毒性高100倍,并易被人体吸收且在体内蓄积,有关含铬化合物的相互转化关系如图甲:

回答下列问题:
(1)从图中信息判断,Cr(OH)3是__________氢氧化物(填写“酸性”、“碱性”或“两性”),相关反应的离子方程式为__________。
(2)图中所示转化过程中需要加入氧化剂的是__________(填写表示转化过程的小写字母)。
(3)在水溶液中橙色的Cr2O72﹣与黄色的CrO42﹣有下列平衡关系:Cr2O72﹣+H2O 2CrO42﹣+2H+
2CrO42﹣+2H+
①向K2Cr2O7稀溶液中加入NaOH溶液后,溶液颜色的变化是__________。
②以铬酸钾(K2CrO4)为原料,电化学法制备重铬酸钾(K2Cr2O7)的实验装置示意图如图乙:阳极室中的电极反应式是 ,阴极室中的KOH的物质的量__________(填写“变大”、“变小”或“不变”)。
(4)CrO3具有强氧化性,热稳定性较差,加热时逐步分解,其固体残留率( ×100%)随温度的变化如图丙所示。
×100%)随温度的变化如图丙所示。
①三氧化铬在稀硫酸环境中氧化乙醇,CrO3变为绿色的Cr2(SO4)3,乙醇被完全氧化为CO2,则其化学方程式是 。
②图中B点所示固体的化学式是 。
(7分)在0.5mol/L的NaHSO3溶液中滴入石蕊,溶液变红。试回答下列问题:
(1)该溶液中HSO3-的电离程度______(填“大于”、“小于”或“等于”)HSO3-的水解程度。
(2)溶液中Na+、HSO3-、H+、OH-、SO32-等离子的浓度由大到小的顺序为。
(3)在Na2SO3溶液中滴入酚酞,溶液变红。若在该溶液中再滴入过量的BaCl2溶液,所观察到的现象是。其原因是(以离子方程式及简要文字说明)。
(12分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g)  2NH3(g) △H=" -92.4KJ/mol" ,据此回答以下问题:
2NH3(g) △H=" -92.4KJ/mol" ,据此回答以下问题:
(1)下列有关该反应速率的叙述,正确的是(选填序号)。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强不能增大活化分子百分数,所以不可以加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
(2)①该反应的化学平衡常数表达式为K=_______________________。
②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越_____ 。
(3)某温度下,若把10 mol N2与30 mol H2置于体积为10 L的密闭容器内,反应达到平衡状态时,测得平衡混合气体中氨的体积分数为20%,则该温度下反应的K=___________(可用分数表示)。能说明该反应达到化学平衡状态的是(填字母)。
a.容器内的密度保持不变 b.容器内压强保持不变
c.υ正(N2)=2υ逆(NH3) d.混合气体中c(NH3)不变
(4)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)_____________。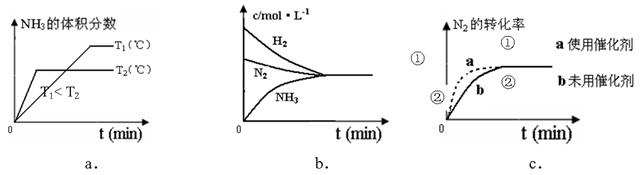
(5)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1mol N2和3 molH2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;
B中NH3的体积分数为b,放出热量Q2 kJ。则:a_____b(填>、=、<), Q1_____ Q2(填>、=、<), Q1_____92.4(填>、=、<)。
(8分)(1)常温下,有0.1mol/L的盐酸和0.1mol/L的醋酸溶液,回答下列问题:
①比较两溶液的pH ,盐酸(填“<” 、“="”" 或 “>”)醋酸,写出醋酸电离的方程式。
②两种酸均能与氢氧化钠反应生成盐,其中醋酸与氢氧化钠反应能生成醋酸钠,实验室现有部分醋酸钠固体,取少量溶于水,溶液呈(填“酸性” 、“中性” 或 “碱性”),其原因是(用离子方程式表示)。
③向醋酸溶液中加入一定量的NaOH溶液,当测得溶液的pH=7时,溶液中离子的浓度大小为
(填字母,下同),当测得溶液的pH<7时,溶液中离子的浓度大小为。
a.c(Na+)>c(CH3COO—)>c(OH—)>c(H+) b.c(Na+) = c(CH3COO—)>c(OH—) =c(H+)
c.c(CH3COO—)>c(Na+)>c(H+)>c(OH—) d.c(Na+)>c(CH3COO—)>c(H+)>c(OH—)
(2)向盛有1mL0.1mol/LMgCl2溶液的试管中滴加2滴2mol/L NaOH溶液,有白色沉淀生成,再滴加2滴0.1mol/LFeCl3溶液,静置。可以观察到的现象是,产生该现象的原因是(用离子方程式或文字表示)。
(6分)已知25℃、101kpa时,一些物质的燃烧热为:
| 化学式 |
CO(g) |
H2(g) |
CH3OH(l) |
CH4(g) |
| △H/(kJ/mol) |
-283.0 |
-285.8 |
-726.5 |
-890.3 |
请回答下列问题。
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式:。
(2)根据盖斯定律完成下列反应的热化学方程式:
CO(g)+ 2H2(g)= CH3OH(l);△H=。
(3)现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5 kJ,则原混合气体中H2和CH4的物质的量之比是:
| A.1∶1 | B.1∶3 | C.1∶4 | D.2∶3 |
标准状况下,1.68L无色无味的可燃性气体在足量氧气中完全燃烧。若将产物通入足量澄清石灰水.得到的白色沉淀质量为15.0g;若用足量碱石灰吸收燃烧产物,增重9.3g。
(1)计算燃烧产物中水的质量:_______________
(2)若原气体是单一的烃类气体,通过计算推断它的化学式:______________________
(3)若原气体是两种等物质的量的气态烃的混合物,请写出它们的结构简式(要求写出两组符合条件的物质的结构简式):______和______、________和_______