用18mol/L浓硫酸配制100mL 1.0mol/L的稀硫酸,若实验仪器有:
A.100mL量筒
B.托盘天平
C.玻璃棒
D.50mL容量瓶
E.10mL量筒
F.胶头滴管
G.50mL烧杯
H.100mL容量瓶
(1)实验时选用的仪器有(填入编号)_____________________。
(2)下列操作使所配溶液的浓度偏高的是(填入编号)_________________。
A.定容时超过刻度线
B.定容时俯视刻度线
C.容量瓶内壁附有水珠而未干燥处理
D.在烧杯中稀释后没有冷却便转移至容量瓶
E.量取浓硫酸时仰视量筒
F.将容量瓶颠倒摇匀后发现液面低于刻度线
如图a、b、c、d是一张浸有饱和食盐水的滤纸,E、F为铂片,其附近滴有两滴石蕊试液。X、Y由Cu、Zn组成。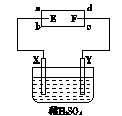
(1)若工作时,E附近出现蓝色,则E为极;F为极;Y为极,Y材料为。
(2)若E、F均为铜片,其余不变,则E、F的电极反应:E极,F极。
如何设计A、B、C、D分别符合下述要求: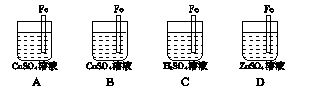
(1)A中Fe棒不溶解但质量增加。
(2)B中Fe棒溶解,但Cu不在Fe上析出。
(3)C中Fe棒不溶于H2SO4。
(4)D中ZnSO4浓度不变。
某化工厂排出的废水中含有氯气和硫酸,为了除去此废水中的游离氯,并使废水变为中性,供使用的试剂有碳酸钠和亚硫酸钠溶液,试回答:
(1)应先向废水中加入溶液,离子方程式为。
(2)然后再向废水中加入溶液,离子方程式为。
硫酸工业生产应考虑综合经济效益问题。
(1)据测算,接触法制硫酸过程中,若反应热都未被利用,则每生产1 t 98%的硫酸需消耗3.6×105 kJ的热量。请通过计算判断,若反应SO2(g)+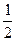 O2(g)
O2(g) SO3;ΔH="-98.3" kJ·mol-1放出的热量能在生产过程中得到充分利用,则每生产1 t 98%的硫酸只需外界提供(或可向外界输出)多少千焦热量?(H2SO4的摩尔质量为98 g·mol-1)
SO3;ΔH="-98.3" kJ·mol-1放出的热量能在生产过程中得到充分利用,则每生产1 t 98%的硫酸只需外界提供(或可向外界输出)多少千焦热量?(H2SO4的摩尔质量为98 g·mol-1)
(2)CuFeS2是黄铁矿的另一成分,燃烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为。
(3)硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度的不同而变化(见下表)。
| 沸腾炉温度/℃ |
600 |
620 |
640 |
660 |
| 矿渣中CuSO4的质量分数/% |
9.3 |
9.2 |
9.0 |
8.4 |
已知CuSO4在低于660 ℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因。
用下列装置可测定SO2转化为SO3的转化率。
(1)根据实验的需要,(Ⅰ)(Ⅱ)(Ⅲ)处应连接合适的装置。请从下面装置中选择合适的装置,将其序号填入以下空格内:(Ⅰ);(Ⅱ);(Ⅲ)。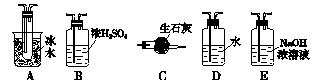
(2)实验时,浓硫酸能顺利地滴入烧瓶中,甲仪器所起作用的原理是。
(3)用大火加热烧瓶时,SO2的转化率会(填“提高”“不变”或“降低”)。
(4)用a mol Na2SO3粉末与足量的浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ装置增重b g,则本实验中SO2的转化率为。