铈、钛、锌、锰虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,反应中CeO2作 剂。在加热条件下,CeCl3易发生水解,无水CeCl3可用加热CeCl3·6H2O和NH4Cl固体混合物的方法来制备。其中NH4Cl的作用是______________ 。
(2)钛(Ti)被誉为“二十一世纪的金属”。
①在高温下,向金红石(主要成分Ti02)与焦炭的混合物中通入Cl2,得到TiCl4和一种可燃性气体。该反应的化学方程式是 。
②加热条件下,镁与TiCl4反应可得到钛,下列气体可以作为保护气的是
A.O2 B.N2 C.C02 D.Ar
(3)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。写出锌和氢氧化钠溶液反应的化学方程式 。
(4)锰及其化合物应用越来越广泛,MnO2是一种重要的无机功能材料。
①已知A~G各物质间的关系如下图,其中B、D为气态单质。
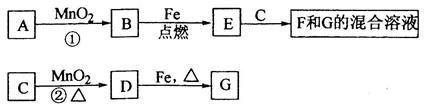
则反应②的离子方程式为_______________________________________。
②制备Mn02的方法之一是以石墨为电极,电解酸化的MnSO4溶液,阳极的电极反应式为 。已知:Ksp[Al(OH)3]=1×10-33,pH=7.1时Mn(OH)2开始沉淀。室温下,欲除去MnSO4溶液中的Al3+(使其浓度小于1×10-6mol·L-1),需调节溶液pH范围为________。
下表为元素周期表的一部分,其中编号代表对应的元素。
① |
||||||||||||||||||||
| ② |
③ |
④ |
⑤ |
⑥ |
||||||||||||||||
| ⑩ |
⑨ |
|||||||||||||||||||
| ⑦ |
⑧ |
|||||||||||||||||||
请回答下列问题:
(1)写出元素⑦的价电子排布图__________ ,⑧的原子结构示意图__________。71号元素属于_______周期,________族,_______区。
(2)若元素①③⑤形成的某化合物中三种元素的质量比为1:6:8,该化合物对氢气的相对密度为15,该分子中心原子的杂化方式为______________。
(3)④和⑥形成的分子构型___________。
(4)③的某种同素异形体被称为混合型晶体,具有平面层状结构。该晶体中含有的作用力为______________________________________。
(5)②与⑤形成的化合物的熔点___________②与⑨形成化合物的熔点(填“高于”或“低于”)
(6)⑩的第一次出现突变的电离能数据是I2,则它的下一个出现突变的电离能数据是_______。
已知反应:2H2CrO4 + 3H2O22Cr(OH)3 + 3O2↑+ 2H2O该反应中H2O2只发生如下变化过程:H2O2→O2
(1)该反应中的还原剂是
(2)用单线桥法表示反应中电子转移的方向和数目
2H2CrO4 + 3H2O22Cr(OH)3 + 3O2↑+ 2H2O
(3)如反应中转移了0.6mol电子,则产生的气体在标准状况下体积为
写出下列物质间反应的离子方程式:
(1)氯化铝溶液中加入过量氨水;
(2)氢氧化钡溶液与硫酸铜溶液混合;
(3)少量NaHSO4溶液与过量氢氧化钡溶液。
在标准状况下,①4g氢气 ②33.6 L甲烷 ③6.02×1023个水分子,含分子数最多的是(填序号,下同),含原子数最多的是,质量最大的是,体积最小的是。
①常温下,0.05mol/L硫酸溶液中,C(H+)=mol/L,
水电离的C(H+)=mol/L
②某温度,纯水中C(H+)==3×10-7mol/L,则:
纯水中C(OH-)="=" mol/L,此时温度(填“高于”“低于”或“等于”)25℃。若温度不变,滴入盐酸后C(H+)=5×10-4mol/L,
则溶液中C(OH-)= mol/L,由水电离的C(H+)="=" mol/L。