氯元素是生产生活中常见的非金属元素。
(1)将Cl2通入NaOH溶液中得到以NaClO为有效成分的漂白液,写出该反应的离子方程式 ;不直接用Cl2作漂白剂的原因是 (写出两条)。
(2)使用Cl2为自来水消毒时,会与水中的有机物生成对人体有害的有机氯化物。下列物质中可以替代Cl2为自来水杀菌消毒的是 (填字母序号)。
a.臭氧 b.NH3 c.明矾 d.ClO2
(3)生物质混煤燃烧是当今能源燃烧利用的最佳方式之一,但生物质中氯含量较多,燃烧过程中会形成金属氯化物(如NaCl)和Cl2等物质,对金属炉壁造成腐蚀。
①NaCl和Cl2中化学键的类型分别是 和 。
②燃煤过程中生成的SO2会与NaCl等物质发生反应,生成硫酸盐和Cl2。若生成Cl2 22.4 L(标况)时转移电子数为4×6.02×1023,该反应的化学方程式是 。
③已知:2H2O2(l)=2H2O(l)+O2(g) ΔH1 = -196.46 kJ·mol-1
H2(g)+1/2O2(g)= H2O(l) ΔH2 = -285.84 kJ·mol-1
Cl2(g)+H2(g)=2HCl(g) ΔH3 = -184.60 kJ·mol-1
在催化剂作用下,用H2O2(l)可除去上述燃烧过程中产生的Cl2。依据上述已知反应,写出该反应的热化学方程式: 。
甲醇是重要的化学工业基础原料和清洁液体燃料。工业上可利用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:
| 化学反应 |
平衡常数 |
温度℃ |
|
| 500 |
800 |
||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) |
K1 |
2.5 |
0.15 |
②H2(g)+CO2(g) H2O (g)+CO(g) H2O (g)+CO(g) |
K2 |
1.0 |
2.50 |
③3H2(g)+CO2(g) CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) |
K3 |
(1)反应②是(填“吸热”或“放热”)反应。
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如右图所示。则平衡状态由A变到B时,平衡常数K(A)K(B)(填“>”、“<”或“=”)。
(3)据反应①与②可推导出K1、K2与K3之间的关系,则K3= __ (用K1、K2表示)。500℃时测得反应③在某时刻,H2(g)、CO2(g)、CH3OH(g)、H2O (g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15, 则此时 V正V逆(填“>”、“<”或“=”)。
(4)在3 L容积可变的密闭容器中发生反应②,已知c(CO)-反应时间t变化曲线Ⅰ如图所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。
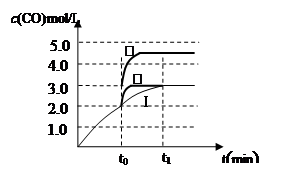
当曲线Ⅰ变为曲线Ⅱ时,改变的条件是。
当曲线Ⅰ变为曲线Ⅲ时,改变的条件是。
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将a mol/L的醋酸与b mol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)= c(CH3COO-),用含a和b的代数式表示该混合溶液中醋酸的电离常数为。
在构成宇宙万物的一百多种元素中,金属约占了80%,它们在现代工业和新材料、新技术研究中具有至关重要的意义。现有a、b、c、d四种金属元素,a是人体内含量最多的金属元素,b是地壳中含量最多的金属元素,c是海水中含量最多的金属元素,d是人类冶炼最多的金属元素。
(1)元素a在元素周期表中的位置为 ;
(2)下列可以证明b、c金属性强弱的是 。
A.最高价氧化物对应水化物的溶解性:b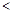 c B.单质与水反应的剧烈程度:b
c B.单质与水反应的剧烈程度:b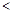 c
c
C.相同条件下,氯化物水溶液的pH值:b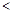 c D.c可以从b的氯化物水溶液中置换出b
c D.c可以从b的氯化物水溶液中置换出b
(3)b的阳离子与Yn-的电子数相同, Y所在族各元素的氢化物的水溶液均显酸性,则该族元素的氢化物中沸点最低的是________。(填化学式)
(4)b电池性能优越,b一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
①该电池的总反应化学方程式为_______________________________________________;
②用b电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为______________________,此时向溶液中加入8gCuO固体后可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为___________L。
(5)人类冶炼d的时候一般得到的是d的合金,潮湿环境中其表面会产生一层水膜,从而发生腐蚀。下列关于该腐蚀的说法正确的是 。
A.腐蚀过程中,一定会有气体放出
B.腐蚀过程中,水膜的碱性会增强
C.在酸性条件下,负极的电极反应式为:2H++2e-→H2
D.与电源的负极相连,可以防止发生这种腐蚀
(6)d单质在高温下会与水蒸气反应生成一种黑色固体和一种易燃性气体,且每生成1 mol该易燃气体放出37.68 kJ热量,请写出此反应的热化学方程式: 。
(15分)松油醇是一种调味香精,它是由α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(下式中的18是为了区分两个羟基而人为加上去的)经下列反应制得: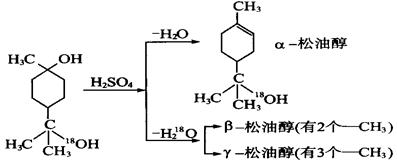
试回答:
(1)α-松油醇的分子式为。
(2)α-松油醇所属的有机物类别是。
A.醇 B.酚C.饱和一元醇
(3)α-松油醇能发生的反应类型是。
A.加成 B.水解 C.氧化
(4)γ-松油醇的结构简式为。
(5)在许多香料中松油醇还有少量的以酯的形式出现,写出RCOOH和α—松油醇反应生成酯的化学方程式:。
(6)A物质六元环上的一氯代物有种。
A.2 B.3C.4 D.5
(15分)向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续加氨水,难溶物溶解,得到深蓝色的透明溶液;若加入极性较小的溶剂(如乙醇),将析出深蓝色的晶体。 I.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
I.在化学实验和科学研究中,水是一种最常用的溶剂。水是生命之源,它与我们的生活密切相关。
(1)写出与H2O分子互为等电子体的微粒________(填1种)。
(2)水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是。
| A.氧原子的杂化类型发生了改变 | B.微粒的形状发生了改变 |
| C.微粒的化学性质发生了改变 | D.微粒中的键角发生了改变 |
(3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞示意图(未按顺序排序)。与冰的晶体类型相同的是(请用相应的编号填写)。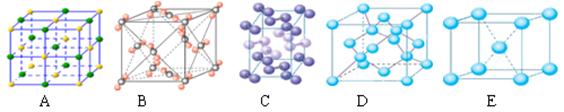
II.胆矾晶体是配制波尔多液的主要原料,波尔多液是一种保护性杀菌剂,广泛应用于树木、果树和花卉上。
(4)写出铜原子价电子层的电子排布式,与铜同一周期的副族元素的基态原子中最外层电子数与铜原子相同的元素有(填元素符号)。
(5)实验时形成的深蓝色溶液中的阳离子内存在的全部化学键类型有 ____。
(6)实验过程中加入C2H5OH后可观察到析出深蓝色[Cu(NH3)4]SO4·H2O晶体。实验中所加C2H5OH的作用是 ____________。
(I)过氧化尿素[CO(NH2)2·H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如下: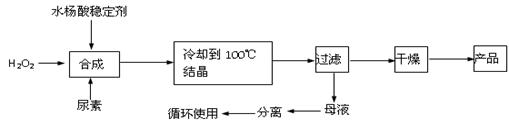
试回答下列问题:
(1)实际生产中需控制n(H2O2)∶n[CO(NH2)2]=1.2∶1,并控制合成温度在25~30℃,其主要原因是。
(2)从母液中分离出H2O2和尿素,采用的操作是 。
(a)盐析过滤 (b)分液过滤 (c)减压蒸馏结晶 (d)常压蒸馏萃取
(II)某硝酸厂附近的空气主要污染物为氮的氧化物,为了保护环境和综合利用,可采用氨-碱两级吸收法,此法兼有碱吸收和氨吸收两法的优点,其吸收工艺流程如下: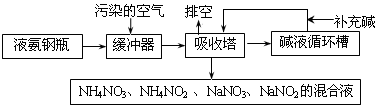
(1)排空物质的主要成分为____________________________。
(2)进入吸收塔以前加一个缓冲器的目的是________________________________。
(3)从吸收塔排出的混合液用途之一为________________ 。
(4)空气的主要污染物为硫的氧化物和氮的氧化物.研究人员设计了同时净化废气中二氧化硫和氮的氧化物的方法,将其转化为硫酸和硝酸,工艺流程如下:
则①和②分别为(写化学式)________________。