(1)自然界Cr主要以+3价和+6价存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬。完成并配平下列离子方程式:
__Cr2O72-+__SO32-+__ =__Cr3++__SO42-+ __H2O
=__Cr3++__SO42-+ __H2O
(2)为测定NiSO4·xH2O晶体中x的值,称取26.3 g晶体加热至完全失去结晶水,剩余固体15.5 g,列式计算x的值等于 。
(3)某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作和有关图象如图所示:

请回答下列问题:
①实验中需配制1.0mol/L的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为
③根据上述3组实验可以分析废水中一定不存在的离子有: .
④分析图象,在原溶液中c(NH4+)与c(Al3+)的比值为 试确定NO3-是否存在? (填“存在”、“不存在”或“不确定”),若存在,试计算c(NO3-)= (若不存在,此问不必作答).
(1).将质量比为14 :15的N2和NO混合,则混合气体中N2和NO的物质的量之比为______,氮原子和氧原子的个数比为________。
(2).同温同压下,质量相同的五种气体: ① CO2② H2③ O2④ CH4⑤ SO2
所占的体积由大到小的顺序是(填序号,下同)_________________;
密度由大到小的顺序是_________________________________。
(3).VmL Al2(SO4)3溶液中含Al3+ ag,取V/4mL溶液稀释到VmL,则稀释后溶液中的SO42-的物质的量浓度是(单位为mol/L)______________。
(4).有一质量为mg,相对分子质量为M的某种强碱M (OH)2,在一定温度下,完全溶解在水中得到VmL饱和溶液,若此溶液的密度为ρg/cm3,则该溶液中OH-的物质的量浓度为________,溶质的质量分数为________。
某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0。反应物A 的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
B+D在四种不同条件下进行,B、D起始浓度为0。反应物A 的浓度(mol·L-1)随反应时间(min)的变化情况如下表:
| 实验 序号 |
时间 浓度 温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800℃ |
C2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
800℃ |
C3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
| 4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在10至20 min时间内平均速率为mol·(L·min)-1。
(2)在实验2中A的初始浓度C2=mol·L-1,反应经20 min就达到平衡,可推测实验2中还隐含的条件是。
(3)设实验3的反应速率为v3,实验1的反应速率为v1,则v3v1(填“>”“=”或“<”=,且C31.0 mol·L-1(填“>”“=”或“<”=。
写出下列方程式
(1)惰性电极电解硫酸铜溶液:阳极:阴极:
总反应:
(2)酸性条件下的甲烷燃料电池:负极:正极:
(3)铁做阳极,碳做阴极电解饱和食盐水:阳极:阴极:总反应:
(4)池是一种高能电池,它质量轻、体积小,是人造卫星、宇宙火箭、空间电视转播站等的电源。电极材料为Zn 和Ag2O,电解质是KOH.
总反应式:Zn + Ag2O = ZnO + 2Ag
负极:________________________________________________
正极:________________________________________________
第三代混合动力车,可以用电动机、内燃机或二者结合推动车辆。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车或下坡时,电池处于充电状态。
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,生成1 mol水蒸气放热569.1 kJ。则该反应的热化学方程式为________________________________________。
(2)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。镍氢电池充放电原理示意如图,其总反应式为H2+2NiOOH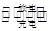 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH________(填“增大”、“减小”或“不变”),该电极的电极反应式为_______________________________________________________________。
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH________(填“增大”、“减小”或“不变”),该电极的电极反应式为_______________________________________________________________。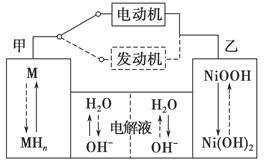
(3)Cu2O是一种半导体材料,可通过如图所示的电解装置制取,电解总反应式为2Cu+H2O Cu2O+H2↑,阴极的电极反应式是_______________________________________________________________。
Cu2O+H2↑,阴极的电极反应式是_______________________________________________________________。
用镍氢电池作为电源进行电解,当电池中有1 mol H2被消耗时,Cu2O的理论产量为________g。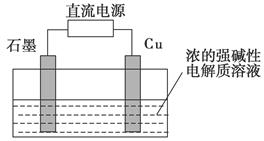
(4)远洋轮船的钢铁船体在海水中易发生电化学腐蚀中的________腐蚀。为防止这种腐蚀,通常把船体与浸在海水里的Zn块相连,或与像铅酸蓄电池这样的直流电源的________(填“正”或“负”)极相连。
如图是一个化学过程的示意图。已知甲池的总反应式为2CH3OH+3O2+4KOH===2K2CO3+6H2O
请回答:
(1)甲池是________池,通入O2的电极作为________极,电极反应式为_______________________________________________________________。
(2)乙池是________池,A电极名称为________极,电极反应式为_______________________________________________________________。
乙池中的总反应离子方程式为______________________________________________________________,
溶液的pH________(填“增大”、“减小”或“不变”)。
(3)当乙池中B(Ag)极的质量增加5.40 g时,甲池中理论上消耗O2________mL(标准状况下)。