在容积不变的密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
2SO3(g) △H<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
| A.图I表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
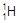 、
、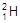 、
、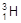 、H+、H2可以表示()
、H+、H2可以表示()
| A.氢的五种同位素 | B.五种氢元素 |
| C.化学性质不同的氢原子 | D.氢元素的五种不同粒子 |
加热N2O5,依次发生的分解反应为:①N2O5(g)  N2O3(g)+O2(g), ②N2O3(g)
N2O3(g)+O2(g), ②N2O3(g) N2O(g)+O2(g).在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为()
N2O(g)+O2(g).在容积为2L的密闭容器中充入8mol N2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为()
| A.10.7 | B.8.5 | C.9.6 | D.10.2 |
把3.0mol M和2.5mol N混合于2.0L的恒容密闭容器中,发生反应
3M (g) + N (g)  xP (g) +2Q (g),5min反应达到平衡,已知M的转化率为50%,P的反应速率为0.15mol·L-1·min-1,则下列说法正确的是()
xP (g) +2Q (g),5min反应达到平衡,已知M的转化率为50%,P的反应速率为0.15mol·L-1·min-1,则下列说法正确的是()
| A.方程式中x=2 |
| B.达平衡后,容器内压强是反应起始时的2倍 |
| C.向容器中再充入3.0molM和2.5molN,达新平衡时Q 的体积分数减小 |
| D.容器内混合气体的密度不再变化和平均相对分子质量不再变化均可作为达到平衡状态的标志 |
已知海水中含有的离子主要有Na+、Mg2+、Cl-、Br-,利用下图装置进行实验探究,下列说法正确的是()

| A.X为锌棒,K置于M,可减缓铁的腐蚀,铁电极上发生的反应为2H++2e-=H2↑ |
| B.X为锌棒,K置于M,外电路电流方向是从X到铁 |
| C.X为碳棒,K置于N,可减缓铁的腐蚀,利用的是外加电流的阴极保护法 |
| D.X为碳棒,K置于N,在X电极周围首先失电子的是Cl- |
X、Y、Z、W、M均为短周期元素,X、Y同主族,X的氢化物和最高价氧化物的水化物能反应生成一种离子化合物,其水溶液显酸性;Z、W、M是第3周期连续的三种元素,其中只有一种是非金属,且原子半径Z>W>M.下列叙述正确的是()
| A.Z是海水中含量最高的金属元素,W是地壳中含量最多的金属元素 |
| B.X、M两元素氢化物的稳定性:X<M |
| C.Z和W的氧化物均可做耐高温材料,M的氧化物可做太阳能电池 |
| D.X、W的最高价氧化物的水化物间反应生成一种可净水的化合物 |