在固态金属氧化物电解池中,高温电解H2O﹣CO2混合气体制备H2和CO是一种新的能源利用方式,基本原理如图所示.下列说法不正确的是( )

| A.X是电源的负极 |
| B.阴极的反应式是:H2O+2e﹣═H2+O2﹣,CO2+2e﹣═CO+O2﹣ |
C.总反应可表示为:H2O+CO2 H2+CO+O2 H2+CO+O2 |
| D.阴、阳两极生成的气体的物质的量之比是1:1 |
下列物质中,属于酸性氧化物但不溶于水的是
| A.Al2O3 | B.CO2 | C.SO3 | D.SiO2 |
下列反应中,氧化剂与还原剂物质的量的关系为1:2的是
| A.4KI+O2+2H2O=4KOH+2I2 |
| B.2CH3COOH+Ca(ClO)2=2HClO+(CH3COO)2 Ca |
| C.I2+2NaClO3=2NaIO3+Cl2 |
D.MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O MnCl2+Cl2↑+2H2O |
下列各组离子:⑴I-、Fe2+、NO3-、H+⑵K+、NH4+、HCO3-、OH- ⑶SO32-、SO42-、K+、OH-⑷Fe2+、Cu2+、SO42-、Cl-⑸Fe3+、SCN-、K+、SO42-⑹H+、K+、AlO2-、HSO3-在溶液中能大量共存且溶液为无色的组别共有
| A.1组 | B.2组 | C.3组 | D.不少于4组 |
全部属于纯净物的是
| A.福尔马林、白酒、食醋 | B.汽油、油脂、酚醛树脂 |
| C.石炭酸、盐酸、冰醋酸 | D.甘油、乙醇钠、氯仿 |
下列有关化学用语的表示方法中正确的是
A.氯元素的原子结构示意图是: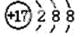 |
| B.N2的结构式:N≡N |
C.原子核内有8个中子的氧原子: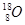 |
D.CO2的电子式是: |