已知:Fe(OH)3不溶于过量氨水,Cu(OH)2溶于过量氨水,转化为[Cu(NH3)4]2+。现有等物质的量组成的铁铜合金0.1mol,研成粉末后,全部投入稀硝酸中,微热使其充分反应,硝酸的还原产物只有NO,由于HNO3用量的不同,溶液中的金属离子和残留固体的成分会有多种情况。下列说法正确的是( )
| A.根据溶液中的金属离子和残留固体的成分最多会有6种情况 |
| B.若金属有剩余,在溶液中再滴入稀硫酸后,金属不会再溶解 |
| C.当合金刚好溶解时,在标准状况下产生2.24LNO |
| D.若合金全部溶解,在溶液中加入过量的氨水,经过滤、洗涤、干燥、充分灼烧,称量得固体5.35g |
下列关于乙烯和乙烷的说法中,不正确的是
| A.乙烯属于不饱和链烃,乙烷属于饱和链烃 |
| B.乙烯分子中所有原子处于同一平面上,乙烷分子中的原子不在同一平面上 |
C.乙烯分子中的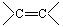 双键比乙烷分子中的C—C单键更稳定,性质更活泼 双键比乙烷分子中的C—C单键更稳定,性质更活泼 |
| D.乙烯能使酸性KMnO4溶液褪色,乙烷不能 |
下列关于有机化合物的说法正确的是
| A.乙醇和乙酸都存在碳氧双键 |
| B.甲烷和乙烯都可以与氯气反应 |
| C.高锰酸钾可以氧化苯和甲烷 |
| D.乙烯可以与氢气发生加成反应,苯不能与氢气加成 |
可以用分液漏斗分离的一组液体混合物是
| A.溴和四氯化碳 | B.苯和溴苯 |
| C.水和硝基苯 | D.苯和汽油 |
下列各组物质中,一定既不是同系物,又不是同分异构体的是
A.CH4和C4H10 B.乙酸和甲酸甲酯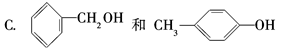 D.苯甲酸和
D.苯甲酸和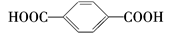
下列有机化合物的分类不正确的是
| A |
B |
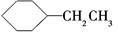 |
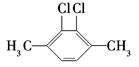 |
| 苯的同系物 |
芳香族化合物 |
| C |
D |
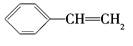 |
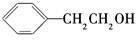 |
| 不饱和烃 |
醇 |