(1)已知在氨水中存在下列平衡:
①向氨水中加入NaOH固体时,平衡向 (填“正反应”“逆反应”或“不”)移动,OH-的浓度 (填“减小”“增大”或“不变”)
②向氨水中加入浓盐酸,平衡向 (填“正反应”“逆反应”或“不”)移动,此时溶液中浓度增大的离子有NH4+(Cl-除外)和
(2)已知某溶液中只存在OH−、H+、NH4+、Cl−四种离子,某同学推测其离子浓度大小顺序有以下几种:
A.c(Cl−)>c(NH4+)>c(H+)>c(OH−) B.c(Cl−)>c(NH4+)>c(OH−)>c(H+)
C.c(NH4+)>c(Cl−)>c(OH−)>c(H+) D.c(Cl−)>c(H+)>c(NH4+)>c(OH−)
①上述关系一定不正确的是______(填序号).
②若溶液中只有一种溶质,则该溶液中离子浓度的大小关系为______(填序号).
③若四种离子浓度关系有c(NH4+)=c(Cl−),则该溶液显______(填“酸性”、“碱性”或“中性”).
(3)常温下,有A、B、C、D四种无色溶液,它们分别是CH3COONa溶液、NH4Cl溶液、盐酸和NaNO3溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。
①则:B是______溶液,C是______.
②常温下若B溶液中c(OH-)与C溶液中的c(H+)相同,B溶液的pH用pHb表示,C溶液的pH用pHc表示.则pHb+pHc= (填某个数)
答案:(1)①逆反应 增大 ②正反应 H+ (2)促进 不变
(3)①B ②A ③中性 (4)①CH3COONa 盐酸 ②14
原子序数之和为16的三种短周期元素的单质X、Y、
Z,常温常压下均为无色气体,在适当条件下X、Y、Z之间可以发生如右图所示的变化。已知B分子组成中Z原子个数比C分子中少一个。请回答下列问题: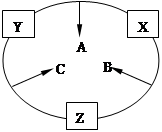
(1)元素X的原子结构示意图
(2)C与X在一定条件下生成化合物A的化学方程式
(3)常温下,C的水溶液能够使红色石蕊试纸变蓝,请用离子方程式表示变蓝的原因
(4)写出A与C反应生成Y和B的化学方程式
(5)加热条件下,C通过装有含X的黑色粉末的硬质玻璃管,黑色粉末变成紫红色,该黑色粉末的化学式 ;发生反应化学方程式为 。
在25 ℃,101 kPa条件下,将15 L O2通入10 L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强。若剩余气体的体积是15 L,则原CO和H2的混合气体中V(CO)=________L,V(H2)=________L。若剩余气体的体积为a L。则原CO和H2的混合气体中V(CO)∶V(H2)=________。若剩余气体的体积为a L,则a的取值范围是 。
如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入NH3 0.4 mol,甲室中充入HCl、N2的混合气体,静止时隔板位置如图所示。已知甲、乙两室中气体的质量差为17.3g。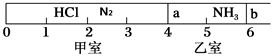
(1)甲室中气体的质量为____ ____。
(2)甲室中HCl、N2的物质的量之比为____ __。
(3)将隔板a去掉,当HCl与NH3充分反应生成NH4Cl固体后(仅发生此反应),隔板b将位于刻度“________”处(填数字,不考虑固体物质产生的压强),此时体系的平均摩尔质量 。
经实验测定,在4 ℃时,水的密度最大,为1 g/mL,请计算一下,4 ℃时1 L水中含有的水分子数为 ,每个水分子的质量为 。
现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂除去溶液中的NaCl和Na2SO4,从而得到纯净的NaNO3溶液。相应的实验过程可用下图表示: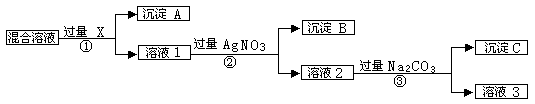
请回答下列问题:
(1)上述实验流程中加入过量的Na2CO3的目的是_________________
(2)按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质;为了解决这个问题,可以向溶液3中加入适量的___________,之后若要获得固体NaNO3需进行的实验操作是___________(填操作名称)。
(3)下列是某学生设计NaCl、Na2SO4、NaNO3混合物中Cl-、SO42-的检验步骤请根据内容填空:
①首先检验 离子,应先加入过量的 ,检验是否加入过量的方法 。
②将所得混合物 (填操作名称),然后在溶液中加入试剂 检验另一离子。