(1)在标准状况下,CO和CO2混合气体的密度是相同条件下H2密度的16倍,则该混合气体的平均相对分子质量为______________ ;若在该条件下混合气体的物质的量为1mol,则其中CO所占的体积为______________ ,CO2所占的质量为__________________ 。
(2)NaHSO4在水中的电离方程式: ___________;
若将NaHSO4与Ba(OH)2在溶液中按物质的量2:1混合,反应的离子方程式是______________
将锌片和铜片用导线相连后一同插入稀硫酸中,导线上便有电流通过。
(1)锌片为______(填“正极”或“负极”),电极反应是。
(2)铜片为__________(填“正极”或“负极”),发生反应(填“ 氧化”或“还原”)。
氧化”或“还原”)。
(3)该原电池工作时,溶液中的SO42-向极移动,铜极上的现象是。
 下边是日照2
下边是日照2 010年9月11日的空气质量日报
010年9月11日的空气质量日报
| 污染指数 |
首要污染物 |
空气质量级别 |
空气质量状况 |
||
| 二氧化硫 |
二氧化氮 |
可吸入颗粒物 |
|||
| 12 |
33 |
66 |
2 |
良 |
(1)首要污染物是
(2)污染指数是
(3)能引起光化学烟雾的是(从表中选)
(4)能引起酸雨的是(从表中选)
丁基橡胶可用于制造汽车内胎,合成丁基橡胶的一种单体A的分子式为C4H8,A与H2加成后得到2—甲基丙烷。完成下列填空:
(1)写出A的结构简式 (2)写出将A通入下列两种溶液后出现的现象。
(2)写出将A通入下列两种溶液后出现的现象。
A通入溴水,A通入溴的四氯化碳溶液
(3)写出分子式为C4H8的烯烃除A以外的同分异构体。
(4)A与某烷烃发生反应生成分子式为C8H18的物质B,B的一卤代物只有4种,且碳链不对称。写出B的结构简式
 能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
能源问题是人类社会面临的重大课题,甲醇是未来重要的能源物质之一。
(1)合成甲醇的反应为:CO(g)+2H2(g) CH3OH(g);下图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H0。(填“>、<或=”下同)
CH3OH(g);下图表示某次合成实验过程中甲醇的体积分数φ(CH3OH)与反应温度的关系曲线,则该反应的△H0。(填“>、<或=”下同)
(2)在某温度下,向一个容积不变的密闭容器中通入2.5mol CO和7.5mol H2,达到平衡时CO的转化率为90%,此时容器内的压强为开始时的倍。
(3)利用甲醇燃料电池设计如图所示的装置:
①则该装置中b为极,写出装置中电解池内发生反应的离子方程式,
②当锌片的质量变化为12.8 g时,a极上消耗的O2 在标准状况下的体积为L。
(4)低碳经济是以低能耗、低污染、低排放为基础的经济模式,其中一种技术是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)="=" C2H4(g)+3O2(g) ΔH=+1411.0 kJ/mol
2CO2(g)+3H2O(l)="=" C2H5OH(1)+3O2(g) ΔH=+1366.8 kJ/mol
则由乙烯水化制乙醇反应的热化学方程式。
物质A有如下图所示转化关系,其中乙为金属单质,常温下,它在G 的浓溶液中发生钝化, F 的溶液中只含有一种溶质(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。请讨论以下两种情况(注:两种情况下各字母代表的物质可能不同)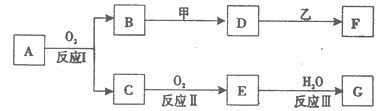
回答下列问题:
(l)第一种情况:用两根玻璃棒分别蘸取 A、G的浓溶液并使它们接近时,有大量白烟生成;甲为焰色反应呈黄色的金属单质; D 和 F 的溶液均呈碱性。则:
①反应Ⅲ的化学方程式为__________________________________________。
②D与乙反应的离子方程式为____________________________________
(2)第二种情况:甲由两种单质直接化合得到;B 为红棕色固体; C为无色气体,是形成酸雨的大气污染物之一 ;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
;D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。则:
①工业上,反应 I的化学方程式为______________________________________
生产设备名称为:
②D和乙反应的离子方程式为____________________________________
③请简述检验D溶液中阳离子的方法。
④若A的相对分子质量为120,反应Ⅰ、Ⅱ、Ⅲ均为完全转化。现取m克含A及少量杂质的样品,按上述过程充分反应后(杂质不参与反应),得到密度为ρg/cm3,溶质质量分数为a% 的G溶液n mL。则该样品中A的质量分数=(列出计算式即可)。