A.《化学与生活》
(1)材料是经济和生态文明建设的重要物资基础
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是________。
②橡胶是制造轮胎的重要原料,橡胶属于_______ (填字母)
A.金属材料 B.无机非金属材料 C.有机高分子材料
③钢铁制品在潮湿的空气中能发生_______腐蚀,发生该腐蚀时的负极电极反应式为________。
(2)防冶环境污染,改善生态环境已成为全球共识
①2013年,全国多个省市出现严重的雾天气,导致雾形成的主要污染物是_____(填字母)
A.O2 B.CO2 C.PM2.5
②采用焚烧处理垃圾进行发电已在江苏投入使用。下列是生活中的常见垃圾;
A.废电池 B.易拉罐 C.玻璃瓶
在焚烧前,除废电池外,还有_______(填字母)应剔除并回收,随意丢弃电池造成的主要危害是_______。
③漂白粉可用于生活用水的杀菌消毒,工业上利用氯气和石灰乳制取漂白粉的化学方程式是_______。
(3)合理膳食,保持营养均衡,是青少年学生健康成长的重要保证。
①维生素C能增强人体对疾病的抵抗能力,促进人体生长发育,中学生每天要补充60mg的维生素C;下列物质含有丰富维生素C的是______(填字母)
A.牛肉 B.辣椒 C.鸡蛋
②青少年及成人缺乏某种微量元素将导致甲状腺肿大,而且会造成智力损害,该微量元素是______(填字母)A.碘 B.铁 C.钙
③蛋白质是人体必需的营养物质,它在人体内最终水解为___________。
(4)材料是人类生存和发展的物质基础,合理使用材料可以改善我们的生活。
①居室装修所使的人造板材会释放出一种挥发性物质,长期接触会引起过敏性皮炎,免疫功能异常,该挥发性物质是_________。
②玻璃是重要的硅酸盐产品,生产玻璃时,石灰石与石英反应的化学方程式为___________。
(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是非通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是▲(填“吸热”或“放热”)反应,NO2和CO的总能量 ▲(填“>”、“<”或“=”)CO2和NO的总能量。

(2)在某体积为2L的密闭容器中充入1.5mol NO2和2mol CO,在一定条件下发生反应:NO2+CO===CO2+NO,2 min时,测得容器中NO的物质的量为0.5 mol ,则:
①该段时间内,用CO2表示的平均反应速率为 ▲
①2 min时,容器内气体的总物质的量为 ▲。
③假设此反应在5 min时达到平衡,则此时容器内气体的总物质的量 ▲(填“大于”、“小于”或“等于”)2 min时容器内气体的总物质的量。
A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D顺序依次增大。A、D同主族;B、D、E三种元素原子的最外层电子数之和为10;E的单质可做半导体材料;C与E两元素形成的化合物可与A、C、D形成的化合物Y发生反应;B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M。1molM中含有42mol电子。回答下列问题:
(1)E元素在周期表中的位置:周期族;化合物M中含有的化学键类型有__________________________;用电子式表示化合物A2C的形成过程:___________________________________________
(2)比较B、C、E形成的气态氢化物的稳定性(用化学式表示):>>;写出C与A形成的18e-化合物的电子式;
(3)写出C与E两元素形成的化合物与Y溶液反应的离子方程式:
____________________________________________________;
(4)以铂作电极,以Y溶液作为电解质溶液,A、C元素的单质分别在两电极上发生原电池反应,则负极上的电极反应式为__________________________。
(1)写出一个能证明还原性Fe比Cu强的离子方程式:
;
(2)根据上述反应设计一个原电池,画出简易装置图(标出电极名称、电极材料、电解质溶液)
;
(3)若该电池中两电极的总质量为60 g,工作一段时间后,取出两电极洗净干燥后称量,总质量为62 g,则反应过程中转移电子的数目为。
某核素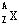 的氯化物XCl2 1.11 g配成溶液后,需用1mol·L-1的硝酸银溶液20 ml才能把氯离子完全沉淀下来。则X的质量数为;若X的核内中子数为20,则37 g XCl2中所含质子的物质的量。
的氯化物XCl2 1.11 g配成溶液后,需用1mol·L-1的硝酸银溶液20 ml才能把氯离子完全沉淀下来。则X的质量数为;若X的核内中子数为20,则37 g XCl2中所含质子的物质的量。
分子中含有10个氢原子的烷烃的分子式是;这种烷烃具有种不同的结构;写出其中没有支链的烃的结构简式,
写出该物质与氯气反应生成一氯代物且氯原子在一端碳原子上的化学方程式并注明反应的类型:_____________________________________________________________________。