氧化剂和还原剂在生产生活中广泛使用。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:
2KMnO4+ 16HBr = 5Br2+ 2MnBr2+ 2KBr+ 8H2O
①其中还原剂为 ,还原产物为
②若有0.8 mol还原剂被氧化,则转移电子的物质的量是
(2)双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN,其中N为﹣3价),化学方程式为:KCN+H2O2+H2O═KHCO3+A↑(已配平)
①生成物A的化学式为
②用双线桥法表示该反应中电子转移的方向和数目:
(3)古老但仍然是最有用的制备联氨(N2H4)溶液的方法如下:
NaClO+ NH3·H2O 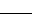 N2H4 + NaCl+ H2O
N2H4 + NaCl+ H2O
①请配平上述化学方程式
②NH3·H2O在上述反应中显示出来的性质是
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(4)人体内所含铁元素以Fe2+和Fe3+的形式存在市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为 ,但Fe2+在酸性条件下很容易被空气中的氧气氧化,写出该反应的离子方程式
某化工厂的废液经测定得知主要含有乙醇,其中还溶有苯酚(熔点:43 ℃)、乙酸和少量二氯甲烷。现欲从废液中回收它们,根据各物质的熔点和沸点,该工厂设计了以下回收的实验方案。
请完成下列问题:
(1)写出试剂A____________、B____________、C____________的化学式:A____________,B____________,C____________;
(2)写出操作D的名称:D________________;
(3)写出回收物①②和G的组成:①______________,②____________,G____________。
已知:
乙烯酮与活泼的氢化物易发生加成反应,如与HCl的反应如下:
从乙酸出发,可发生下图转化:
完成下列问题:
(1)上面乙酸转化图中,将每种类型反应的个数填入空格,取代反应_____________个,加成反应_____________个,消去反应_____________个。
(2)C的结构简式为_______________________,D的结构简式为____________________。
(3)C的同分异构体甚多,其中含1个—OH和四元环(由3个C、一个O构成)的环酯类化合物有_____________种。
(4)写出A D的化学方程式_______________________________________________。
D的化学方程式_______________________________________________。
分子式为C3H6O3的物质有多种同分异构体,请写出符合下列要求的各种同分异构体的结构简式。说明:①不考虑同一碳原子上连两个羟基;②乙炔、苯等分子中同类原子化学环境相同,丙烷、丁烷等分子中同类原子化学环境有两种。
(1)甲分子中没有甲基,且1 mol甲与足量金属Na反应生成1 mol H2。若甲还能与NaHCO3溶液反应,则甲的结构简式为__________________________;若甲还能发生银镜反应,则甲的结构简式为_________________________。
(2)乙分子中所有同类原子的化学环境相同,且不与金属Na反应,则乙结构简式为:_______。
(3)丙分子中碳与氧分别有两种化学环境,氢的化学环境相同,且丙与金属Na不反应,则丙结构简式为__________________________________________。
硫单质通常是一种淡黄色固体,它的蒸气有橙色、无色、红棕色三种,它们都是硫的单质,但每个分子中硫原子个数不同,可用Sx表示。对这三种蒸气的测定结果如下:
(1)橙色蒸气的密度折算成标准状况后是11.34 g·L-1,则它的化学式为________________。
(2)红棕色蒸气的质量是相同状况下同体积空气的6.62倍,则它的化学式为_____________。
(3)无色蒸气是相同状况下氢气密度的64倍,则它的化学式为______________________。
(4)以上三种蒸气都属于硫单质的____________________。
可以从以下角度判断氯元素和硫元素非金属性的强弱:
(1)在元素周期表中,氯元素和硫元素的相对位置是__________________________,根据____________________________规律来判断氯元素和硫元素非金属性的强弱。
(2)二者气态氢化物中______________(填化学式)更易分解,由此可判断氯元素和硫元素非金属性的强弱。
(3)向硫化氢溶液中通入氯气,溶液变浑浊,反应的化学方程式为__________________,说明氯元素的非金属性比硫元素________________(填“强”或“弱”)。
(4)氯气和硫分别与铁形成化合物的化学式为________________和________________,据此也可判断氯元素和硫元素非金属性的强弱。