A.《化学与生活》
Ⅰ.随着生活水平的提高,人们越来越关注自身的健康。以下是探讨化学物质与人体健康的有关问题:
(1)发育出现障碍,患营养缺乏症,这主要是由于摄取蛋白质不足引起的。蛋白质在人体内水解的最终产物是__________
(2)被称为东方神药的青蒿素每年都在挽救全世界无数人的生命,中国女科学家屠呦呦获得2015年诺贝尔生理学或医学奖,以表彰其对治疗疟疾药物青蒿素的研究贡献。

下列有关青蒿素(化学式为C15H22O5)说法不正确的是__________
A.青蒿素易溶于酒精、水等溶剂
B.青蒿素由碳、氢、氧三种元素组成
C.每个青蒿素分子由15个碳原子、22个氢原子、5个氧原子构成
D.青蒿素不可以发生水解反应
E.青蒿素中氢元素的质量分数是22/280
(3)可以帮助流感病人解热镇痛的药物是____________(选填“青霉素”或“阿司匹林”)。胃舒平(氢氧化铝)可用于治疗胃酸过多,请写出有关离子方程式_________________。
Ⅱ材料的不断发展可以促进社会进步。
(1)钢铁是制造航母的主要材料,钢铁在潮湿空气中易发生________腐蚀,其负极反应是__________。请列举一种防止钢铁腐蚀的方法:_________________。
(2)不锈钢丝与棉纤维可织成一种防辐射布料。这种布料属于 (填字母)。
a.合金材料 b.复合材料 c.陶瓷材料
(3)氮化硅是一种新型高温材料,可用于制造汽车发动机。请写出高纯硅和氮气在1300℃时反应制备氮化硅的化学方程式:___________________________________。
Ⅲ 我国新修订的《环境保护法》,使环境保护有了更严格的法律依据。
(1)往燃煤中加入 (填化学式),可大大减少产物中的SO2。
(2)漂白粉用于生活用水的杀菌消毒,漂白粉的有效成份是 (填化学式)。治理废水中的重金属污染物可用沉淀法。例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为 (填化学式)沉淀而除去。
Ⅰ.25℃时,①氢氟酸②醋酸③次氯酸的电离常数分别是3.5×10-4、1.8×10-5、3.0×10-8。请推测:
(1)它们的酸性由强到弱的顺序为______________________(填序号,下同),
(2)相同浓度的溶液中,氢离子浓度最大的是__________,电离程度最小的是_______;
(3)相同浓度的④氟化钠溶液、⑤醋酸钠溶液、⑥次氯酸钠溶液pH的从大到小顺序:___________
Ⅱ.某盐或“类盐”的化学式为XmYn最简结构,将一定量的该盐溶于足量的水时:
(1)若m≠n,测得溶液的pH为5,若该盐只存在一种能水解的离子,则该离子与水反应的离子方程式为________。
(2)若m≠n,测得该盐溶液的pH为9,若该盐只存在一种能水解的离子,则该盐与水反应的离子方程式为____。
粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.15 L 6.0 mol/L盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12 L(标准状况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请回答:
(1)①中引发铝热反应的实验操作是___________,产物中的单质B是_____________。
(2)②中所发生的各反应的化学方程式是_______________________________。
(3)③中所发生的各反应的离子方程式是_______________________________。
(4)若溶液D的体积仍视为0.15 L,则该溶液中c(Mg2+)为________,c(Fe2+)为___________________。
化学研究性学习小组拟通过实验探究“新制的还原性铁粉和过量盐酸反应生成FeCl2还是FeCl3”。请你参与探究并回答有关问题:
(1)一位同学用向反应后的溶液中滴加NaOH溶液的方法来验证溶液中含有Fe2+。①可观察到的实现现象是___________,②反应过程中发生反应的化学方程式是______________。
(2)另一位同学向反应后的溶液中先滴加KSCN溶液,再向其中滴加新制氯水,溶液呈现红色,但当滴加过量新制氯水时,却发现红色褪去。为了弄清溶液红色褪去的原因,同学们查到如下资料:
Ⅰ.铁有一种化合物 称为铁酸盐(含有FeO42-)。
称为铁酸盐(含有FeO42-)。
Ⅱ.SCN-的电子式为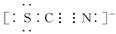
Ⅲ.氯水具有很强的氧化性。
于是同学们提出两种假设:
①第一种假设是:Cl2可将Fe 3+氧化为FeO42-,请写出该离子反应方程式__________。
3+氧化为FeO42-,请写出该离子反应方程式__________。
②第二种假设是:____________,提出该假设的理论依据是
A、B、C、D、E是中学常见的5种化合 物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。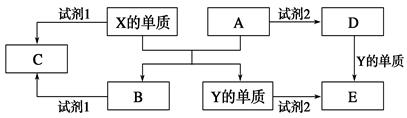
(1)X的单质与A反应的化学方程式是_______________________________。
(2)若试剂1是NaOH溶液,X的单 质与试剂1反应的离子方程式是_____________。
质与试剂1反应的离子方程式是_____________。
(3)若试剂1和试剂2均是稀硫酸。
①检验物质D的溶液中金属离子的方法是___________________________。
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)________________。
③某高效净水剂是由Y(O H)SO4聚合得到的。工业上以E、稀硫酸和亚
H)SO4聚合得到的。工业上以E、稀硫酸和亚 硝酸
硝酸 钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是
钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是
__________________________。
 锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。回答下列问题:
锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成[Zn(NH3)4]2+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为________(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式:_______________________________。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是______________。
①硫酸铝和氢氧化钠 ②硫酸铝和氨水 ③硫酸锌和氢氧化钠 ④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式:______________________________。