下列关于Na2O与Na2O2的说法正确的是
| A.二者阴阳离子个数之比都为2:1 |
| B.二者都能与CO2发生化合反应生成Na2CO3 |
| C.二者都是强氧化剂 |
| D.1molNa2O2与足量盐酸反应,转移电子的物质的量为2mol |
m mol C2H2跟n mol H2在密闭容器中反应,当该可逆反应达到平衡时,生成p mol C2H4。将反应后的混合气体完全燃烧,生成CO2和H2O,所需要氧气的物质的是()
乙醇(CH3CH2OH)和二甲醚(CH3-O-CH3)互为的同分异构体的类型为()
| A.碳链异构 | B.位置异构 | C.官能团异构 | D.顺反异构 |
一种用于制造隐形飞机的材料其主要成分的分子结构如下图,它属于()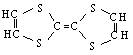
| A.无机物 | B.烯烃 |
| C.高分子化合物 | D.有机化合物 |
某烯烃与H2加成后的产物是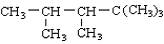 , 则该烯烃的结构式可能有()
, 则该烯烃的结构式可能有()
| A.1种 | B.2种 | C.3种 | D.4种 |
下列叙述正确的是()
①化学反应都遵循质量守恒定律②化学反应都遵循能量守恒定律
③化学反应都有新物质生成④化学反应都伴随着能量的变化
| A.只有① | B.只有①② | C.只有①②③ | D.①②③④ |