下列是对河水的处理步骤:河水→A(明矾)→B(沉淀)→C(过滤)→D(漂白粉)→净水
(l)可以除去悬浮杂质的步骤是 ,题中的“净水”是(纯净物、混合物) 其原因是 。
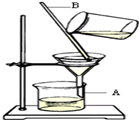
(2)下图是实验室中过滤操作示意图.回答下列问题:图中A的名称是 ,在过滤操作中,B的作用是 。过滤时漏斗下端管口应 .
(3)净水剂漂白粉的有效成分是次氯酸钙,它露置在空气中易与空气中的水和二氧化碳作用转化为难溶的碳酸钙和次氯酸而失效,试写出该变化的文字表达式 ;已知高铁酸钠(Na2FeO4)也是目前广泛被应用的净水剂,其中铁元素的化合价是 。
学习化学知识后,观察物质世界就要从化学视角看。
水是一种重要的物质,在日常生活和实验室中有着不可替代的作用。请按要求回答下列问题:
(1)从组成角度看:水是由组成的,世界上形形色色的物质都是由一百余种元素经过不同组合而形成的。
(2)从微粒角度看:水是由构成的,构成物质的基本微粒有分子、原子、离子。
(3)从变化角度看:化学变化不但生成新物质而且还伴随能量变化。
①水通电分解生成未来最理想的能源——氢气,是将能转化为化学能,但该方法不节能,需要寻找更为有效的节能方法,以促进水的分解;②水参加植物光合作用的化学方程式为:6CO2+6H2O  6O2+X,则X的化学式:。
6O2+X,则X的化学式:。
(4)从资源角度看:水是生命之源。看到如图漫画,你的感想是:(解读漫画或写一则节水广告或一条节水措施)。
今年长江中下游地区遭遇了百年罕见的干旱,在我市,辰溪、麻阳两县旱情尤为严重
(1)写出水的分子式;
(2)干枯的池塘时时散发着恶臭,你能闻到臭味的主要原因是;
(3)任写一条水的作用;
(4)请你写出一条节约用书的做法;
(5)对含碎菜叶、泥沙等的生活用水,采用操作后,可再利用于冲厕所、浇花等。
(6)排放含磷洗衣粉的污水可造成水质恶化,这里的“磷”是指;(选填“原子”、“离子”、“分子”、“元素”)
(7)常用来检验硬水和软水。
2011年3月日本发生9.0级大地震,造成数百万人饮水困难。完成下列各题:
⑴化学式H2O的意义是(答一点即可)。
⑵“水是生命之源”,饮用酸碱过大或硬度过大的水都不利于人体健康。可用测定水的酸碱度。检验水是硬水还是软水,可用的物质是。请你说出生活中使硬水软化的一种常用方法。
小发收集到一瓶浑浊的河水,他要模拟自来水厂的净水过程,最终制成蒸馏水。其实验过程如下所示。请回答以下问题。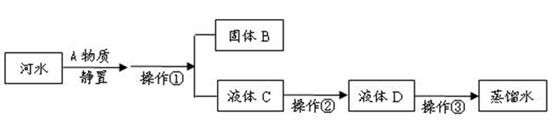
(1)A物质的名称 ,操作①的名称是,若经过操作①后,所得液体C中仍有浑浊,其原因可能是(填写序号);。
a.漏斗内的滤纸有破损缘 b.漏斗下端未靠在烧杯内壁c.漏斗内液面高于滤纸的边
(2)操作②应选用的装置是(填序号),该过程主要是变化(填“物理”或“化学”)。
(3)小刚取少量液体D于试管中,加入少量肥皂水,振荡,发现有较多浮渣产生,说明液体D是水。操作③应选用的装置是(填序号),经过操作③以后,小刚重复上述实验,他观察到的实验现象是


(Ⅰ)(Ⅱ)(Ⅲ)
2008年“中国水周”活动的宣传主题为“发展水利,改善民生”。
(1)①水(填“属于”或“不属于”)六大类营养素之一。②保持水的化学性质的最小粒子是。
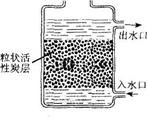
(2)如图是活性炭净水器示意图,其中活性炭的作用是:不仅可以的物质,还可以的杂质。