分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是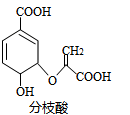
| A.分子中含有2种官能团 |
| B.可与乙醇、乙酸反应,且反应类型相同 |
| C.1摩尔分枝酸最多可与3摩尔氢氧化钠发生中和反应 |
| D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同 |
T℃,向5.0 L恒容密闭容器中充入1.0 molSO3气体,发生反应:2SO3(g)  2SO2(g)+O2(g)
2SO2(g)+O2(g)
△H="+196" kJ/mol,一段时间后达到平衡,测得此过程中从外界共吸收了19.6 kJ的热量。当温度度不变时,改变某一条件,下列结论正确的是
常温下,向20.00 mL 0.100 mol/LCH3COONa溶液中逐滴加入0.1 000 mol/L盐酸,溶液的pH与所加盐酸体积的关系如右下图所示(不考虑挥发)。下列说法正确的是

下列根据实验操作和现象所得出的结论正确的是
短周期元素T、X、Y、Z的原子序数依次增大,T与Z属于同一主族,X、Y、Z最高价氧化物对应的水化物两两之间都能反应,且X、Y、Z原子最外层电子数之和等于X的原子序数。则下列说法正确的是
| A.简单离子半径大小顺序:rT>rX>rY |
| B.T与Z的最高正化合价相等 |
| C.室温下,单质Y不能与浓硫酸反应 |
| D.用电解法可制得T、X、Y的单质 |
甲酸香叶酯是一种食品香料.可以由香叶醇与甲酸发生酯化反应制得。
下列说法中正确的是
| A.香叶醇的分子式为CllHl8O |
| B.香叶醇在浓硫酸、加热条件下可发生消去反应 |
| C.1 mol甲酸香叶酯可以与2 molH2发生加成反应 |
| D.甲酸香叶酯分子中所有碳原子均可能共平面 |