已知反应:2SO2(g)+O2(g) 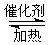 2SO3(g) ΔH<0。某温度下,将2 mol SO2和
2SO3(g) ΔH<0。某温度下,将2 mol SO2和 1 mol O2置于10 L密闭容器中,反应达平衡后
1 mol O2置于10 L密闭容器中,反应达平衡后 ,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是
| A.由图甲知,A点SO2的平衡浓度为0.4 mol·L-1 |
| B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2 |
| C.达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
D.压强为0.50 MPa时不同温度下 SO2转化率与温度关系如丙图,则T2>T1 SO2转化率与温度关系如丙图,则T2>T1 |
下列有关反应热的说法中正确的是
| A.一个化学反应是否能在常温下发生与该反应的△H值的大小没有必然联系 |
| B.中和热△H=" -" 57.3kJ·mol-1,所以1.00L 1.00mol·L-1H2SO4与稀的NaOH溶液恰好完全反应放出57.3kJ的热量 |
| C.用等体积的0.50mol·L-1盐酸、0.55mol·L-1NaOH溶液进行中和热测定的实验,会使测得的值偏大 |
| D.在101KPa时,1molCH4完全燃烧生成CO2和水蒸气放出的热量就是CH4的燃烧热 |
强酸与强碱的稀溶液发生中和反应的热效应:H+(aq)+OH-(aq)=H2O(l);△H=-57.3k J/mol,向1L0.5mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓H2SO4;③稀硝酸,恰好完全反应的热效应△H1、△H2、△H3的关系正确的是
J/mol,向1L0.5mol·L-1的NaOH溶液中加入下列物质:①稀醋酸;②浓H2SO4;③稀硝酸,恰好完全反应的热效应△H1、△H2、△H3的关系正确的是
| A.△H1>△H2>△H3 | B.△H1<△H3<△H2 |
| C.△H1=△H3>△H2 | D.△H1>△H3>△H2 |
可逆反应H2(g)+I2(g)  2HI(g)达到平衡时的标志是
2HI(g)达到平衡时的标志是
| A.混合气体密度恒定不变 | B.混合气体的颜色不再改变 | C.H2、I2、HI的浓度相等 |
| D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等 |
下列各组热化学方程式中,△H1>△H2的是
①C(s)+O2(g)===CO2(g) △H1 C(s)+1/2O2(g)="==CO(g)" △H2
②S(s)+O2(g)===SO2(g) △H1 S(g)+O2(g)===SO2(g) △H2
③H2(g)+1/2O2(g)===H2O(l) △H1 2H2(g)+O2(g)===2H2O(l) △H2
④CaCO3(s)===CaO(s)+CO2(g) △H1 CaO(s)+H2O(l)===Ca(OH)2(s) △H2
| A.① | B.④ | C.②③④ | D.①②③ |