根据下图海水综合利用的工业流程图,判断下列说法正确的是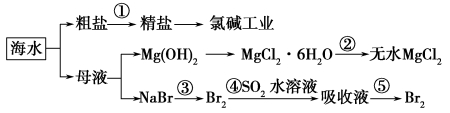
已知:MgCl2·6H2O受热生成Mg(OH)Cl和HCl气体等。
| A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为: NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 |
| B.在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.从能量角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 |
| D.从第③步到第④步的目的是为了浓缩富集溴 |
某溶液可能含有Cl-、SO42-、CO32-、NH4+、Fe3+和K+。取该溶液100mL,加入过量NaOH溶液并加热,得到0.02mol气体,同时产生红褐色沉淀,将过滤洗涤后的沉淀灼烧得到1.6g固体;向上述滤液中加足量BaCl2溶液,得到4.66g不溶于盐酸的沉淀。下列说法正确的是
| A.该溶液中最多存在4种离子 |
| B.该溶液中不能确定是否存在CO32- |
| C.该溶液中一定存在Cl-、且c(Cl-)≥0.4mol∙L-1 |
| D.该溶液可由KCl、(NH4)2SO4和FeCl3配制而成 |
向FeCl3、CuCl2混合溶液中通入H2S和O2的混合气体可回收S,其转化关系如右图。相关说法不正确的是
| A.反应I的基本反应类型是复分解反应 |
| B.反应II中每生成1molS需要2molFeCl3 |
| C.在转化过程中能循环利用的物质有FeCl2和CuCl2 |
| D.在转化过程中化合价不变的元素只有Cu和Cl |
利用右图装置进行下列实验,不能得出相关实验现象的是
| 选项 |
① |
② |
③ |
④ |
| A |
浓盐酸 |
Na2SO3 |
BaCl2溶液 |
出现浑浊 |
| B |
稀盐酸 |
石灰石 |
饱和Na2CO3溶液 |
出现浑浊 |
| C |
浓氨水 |
生石灰 |
酚酞溶液 |
出现红色 |
| D |
醋酸 |
贝壳 |
澄清石灰水 |
先浑浊后澄清 |
NA为阿伏加德罗常数的值。下列说法正确的是
| A.标准状况下,3.36L氧气与3.2g硫反应,生成SO2分子数为0.1NA |
| B.1L0.1mol∙L-1氨水中NH3∙H2O分子数为0.1NA |
| C.标准状况下,1.12LCl2发生反应转移的电子数一定为0.1NA |
| D.10g46%酒精(C2H5OH)中含氧原子总数为0.1NA |
下列离子能满足相应要求的是
| 选项 |
离子组 |
要求 |
| A |
K+、CO32-、SO42-、Cl- |
c(K+)<c(Cl-) |
| B |
Na+、CO32-、NO3-、I- |
滴加盐酸立刻有气体生成 |
| C |
Mg2+、Cl-、Na+、SO42- |
滴加氨水立刻有沉淀生成 |
| D |
NH4+、SO42-、Na+、H+ |
滴加烧碱溶液立刻有气体生成 |