下列关于教材中的各项说法错误的一项是
| A.在化学反应中,反应物转化为生成物的同时,必然发生能量的变化 |
| B.氮肥包括铵态氮肥、硝态氮肥和尿素 |
| C.在书写热化学方程式时应标明反应物及生成物的状态,无需标明反应温度和压强 |
| D.医疗上用的石膏绷带是利用熟石膏与水混合成糊状后很快凝固的性质 |
设NA为阿伏加德罗常数的值,下列叙述正确的是()
| A.标准状况下, 22.4L苯含有C—H数目为6NA |
B.常温下,1L1mol/L FeCl3溶液中,含Cl-数目小于3NA |
C.7.8g Na2O2晶体中含有的阴离子数目为0.1NA |
D.在2NaOH+2F2=OF2+2NaF+H2O反应中,每生成1mol OF2,反应转移电子数为2NA |
下列有关物质的性质或应用的说法不正确的是()
| A.硅是人类将太阳能转变为电能的常用材料 |
| B.氢氧化镁和氢氧化铝是常见的阻燃剂,它们分解时发生吸热反应 |
| C.将海水直接电解可获得 Mg及Cl2等单质 |
D.硫酸铜和石灰乳形成的石硫合剂是 农药,作用机理是铜盐能使蛋白质变性 农药,作用机理是铜盐能使蛋白质变性 |
下列说法中用离子方程式表达正确的是()
| A.用含氢氧化铝的药物治疗胃酸过多症:OH-+H+=H2O |
| B.用亚硫酸钾溶液吸收硫酸工业尾气中的SO2:SO2+SO32-+H2O=2HSO3- |
| C.右图所示电池的反应: Cu2++2Ag=Cu+2Ag+ |
| D.用稀硫酸洗涤沾在试管壁上的氧化亚铜:Cu2O+2H+=2Cu2++H2O |
下列表述正确的是()
A.CO2的电子式为: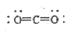 |
B.6CO2+6H2O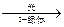 C6H12O C6H12O 6+6O2,该变化中光能直接转变为化学能 6+6O2,该变化中光能直接转变为化学能 |
C.CO2(g)+C(s) 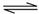 2CO(g) 2CO(g)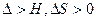 ,该反应常湿下能自发进行 ,该反应常湿下能自发进行 |
D.CO2水溶液呈酸性的原因是CO2+H2O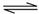 H2CO3 H2CO3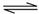 2H++CO32- 2H++CO32- |
化学是在原子、分子水平上研究物质的组成、结构、性质、变化、制备和应用的自然科学。下列不属于化学研究发展方向或说法不正确的是()
| A.高铁酸钾广泛用于废水的净化处理,因为它具有强还原性 |
B.最近合成117号元素的反应为: ,该变化不属于化学变化 ,该变化不属于化学变化 |
| C.“原子经济”和“零排放”是绿色化学和化工的发展目标 |
D.最近在星际介质中发现的分子薏( ),该分子中所有原子可以处于同一平面 ),该分子中所有原子可以处于同一平面 |