镁化合物具有广泛用途,请回答有关镁的下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的______________,还生成少量的______________(填化学式);
(2)将生成的产物加入水中,其中一种产物可与水生成难溶于水的白色沉淀和能使红色石蕊试纸变蓝的气体,请写出该反应方程式 。
(1) 把除去氧化膜的铁丝投入到盛有稀硫酸的试管中,产生氢气的速率变化情况如图所示图中t1~t2速率变化的主要原因是,t2~t3速率变化的主要原因是。
(2)甲、乙、丙、丁是四种短周期元素,乙原子中K层与M层电子数相等;甲原子的核外电子数比乙原子核外电子数少1;丙原子的最外层电子数是次外层电子数的2倍;丁原子核电荷数比丙原子核电荷数多2。请回答:
①甲的单质与水反应的离子方程式为;②乙元素在周期表中的位置为;③丙元素的最高价氧化物的电子式为;④甲与丁两种元素可组成的具有强氧化性的物质是。(填化学式)
(3)某元素R,它的最高价含氧酸的阴离子是RO4ˉ,则其气态氢化物的化学式是。
(7分)现有7瓶失去标签的液体,已知它们是有机试剂,可能是:①乙醇、②乙酸、③苯、④乙酸乙酯、⑤油脂、⑥葡萄糖溶液、⑦蔗糖溶液。现通过如下实验步骤来确定各试剂瓶中所装的液体:
| 实验步骤和方法 |
实验现象 |
| ①把7瓶液体分别依次标号A、B、C、D、E、F、G后,闻气味 |
只有F、G两种液体没有气味 |
| ②各取少量于试管中加水稀释 |
只有C、E、D三种液体不溶解而浮在水面上 |
| ③分别取少量7种液体于试管中加新制Cu(OH)2悬浊液并加热 |
只有B使沉淀溶解,F中产生砖红色沉淀 |
| ④各取少量C、E、D于试管中,加稀NaOH 溶液并加热 |
只有C仍有分层现象,且在D的试管中闻 到特殊香味 |
(1)试给它们的试剂瓶重新贴上标签,其中:
A____________, C____________, E________,F___________,G________。
(2)写出D与NaOH溶液的化学反应方程式: ____________________________
已知A的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
请回答下列问题:
(1)B、D分子中的官能团名称分别是__________、__________。
(2)写出下列反应的化学方程式,并注明反应类型:
②____________________,___________;④____________________,___________。
(3)在实验室利用B和D制备E的实验中,若用1mol B和1 mol D充分反应,能否生成1mol E_________,原因是__________。
(4)若184gB和120gD反应能生成106gE,则该反应的产率______________________。
五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。A原子的最外层电子数比次外层电子层多3个。E周期序数等于E原子最外层电子数。根据以上信息回答下列问题:
(1)A、B、C、D、E五种元素的原子半径由小到大的顺序是(用元素符号填写)
(2)乙物质中存在的化学键类型是。
(3)选用恰当的试剂除去D中少量的E,写出发生反应的化学方程式
(4)化合物乙的电子式
(5)将D、E的单质插入NaOH溶液中,构成原电池,其负极反应是
(14)已知:①双键在链端的烯烃发生硼氢化一氧化反应,生成的醇羟基在链端:
R-CH=CH2 R-CH2CH2OH
R-CH2CH2OH
②RCH2CHO +R'CH2CHO 
化合物M是一种香料,可用如下路线合成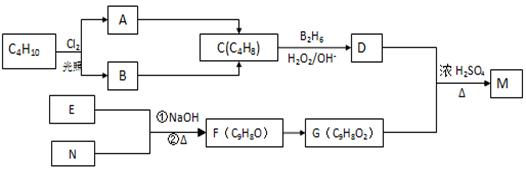
已知:核磁共振氢谱显示E分子中有两种氢原子,F为芳香化合物。请回答下列问题:
(1) 写出反应A→C的反应条件:___________ __________。
(2). 原料C4H10的名称是_________ _____(系统命名)。
(3) 写出M的结构简式:________ ___。
(4) 写出E和N生成F的化学方程式:__________________________。
(5) 写出D和G生成M的化学方程式:_______ __________________。