根据价层电子对互斥理论判断下列分子或离子中空间构型是V形的是 (填写序号)
a.H3O+ b.H2O c.NO2+ d.NO2﹣
(2)已知FeCl3的沸点:319℃,熔点:306℃,则FeCl3的晶体类型为 .P可形成H3PO4、HPO3、H3PO3等多种酸,则这三种酸的酸性由强到弱的顺序为 (用化学式填写)
(3)原子序数小于36的元素Q和T,在周期表中既处于同一周期又位于同一族,且原子序数T比Q多2.T的基态原子外围电子(价电子)排布式为 Q2+的未成对电子数是 .
(4)如图1是从NaCl或CsCl晶体结构图中分割出来的部分结构图,判断NaCl晶体结构的图象是图1中的 .
(5)[Cu(NH3)4]2+配离子中存在的化学键类型有 (填序号).
①配位键②金属键③极性共价键④非极性共价键⑤离子键⑥氢键,
若[Cu(NH3)4]2+具有对称的空间构型,且当[Cu(NH3)4]2+中的两个NH3被两个Cl﹣取代时,能得到两种不同结构的产物,则[Cu(NH3)4]2+的空间构型为 (填序号)
①平面正方形②正四面体③三角锥形④V形.
(6)X与Y可形成离子化合物,其晶胞结构如图2所示.其中X和Y的相对原子质量分别为a和b,晶体密度为ρg/cm3,则晶胞中距离最近的X、Y之间的核间距离是 cm(NA表示阿伏伽德罗常数,用含ρ、a、b、NA的代数式表达)

利用从冬青中提取出的有机物A合成抗结肠炎药物Y及其他化学品,合成路线如下图:
根据上述信息回答:
(1)D不与NaHCO3溶液反应,D中官能团的名称是,B→C的反应类型是。
(2)写出上图中A生成B和E的化学反应方程式。下
(3)写出上图中E转化为F的化学方程式。
(4)A的同分异构体I和J是重要的医药中间体,在浓硫酸的作用下I和J分别生产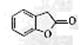 和
和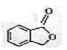 ,鉴别I和J的试剂为。
,鉴别I和J的试剂为。
(5)A的另一种同分异构体K用于合成高分子材料,K可由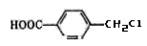 制得,
制得,
写出K在浓硫酸作用下生成的聚合物的结构简式。
X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 |
相关信息 |
| X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z |
Z和Y同周期,Z的电负性大于Y |
| W |
W的一种核素的质量数为63,中子数为34 |
(1)Y元素位于周期表中区,该元素原子核外共有种不同运动状态的电子。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键,该分子中中心原子的杂化类型为。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子外围电子排布式是 。
(4)请写出元素W的单质与元素Y的最高价氧化物对应水化物的浓溶液在一定条件下发生反应的化学方程。
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
此反应的热化学方程式是 。
下表是A、B、C、D、E五种有机物的有关信息;
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为;写出在一定条件下,A生成高分子化合物的化学反应方程式。
(2)写出B在浓硫酸作用下,与浓硝酸反应的化学方程式。
(3)C与E反应能生成相对分子质量为100的酯,其化学反应方程式为。
(4)写出由C氧化生成D的化学反应方程式。
现有A、B、C、D四种短周期元素(零族除外),请根据信息回答下列问题。
| 元素 |
A |
B |
C |
D |
| 性质或结构信息 |
元素非金属性较强,其最高价氧化物对应的水化物为强酸,但其单质稳定,常作保护气。 |
原子核外电子占了4个轨道 |
原子半径仅比氢原子大,其氢化物溶于水形成弱酸 |
原子核外有5种不同能量的电子,且s电子数比p电子数少1个 |
(1)A元素原子的核外电子排布式为:。
(2)写出C元素的单质与水反应的化学方程式;A、C两元素的氢化物的稳定性强弱是>(用化学式表示)。
(3)D元素最高价氧化物对应的水化物呈(选填“酸性”、“碱性”或“两性”)。
(4)B元素最简单的氢化物分子为分子(选填“极性”或“非极性”)。4g该氢化物在空气中完全燃烧生成液态水时,放出222.575kJ热量,写出表示该氢化物燃烧热的热化学方程式。
有短周期元素A、B、C、D、E,已知
①常温下,A元素的单质在空气或浓硫酸中,表面都能生成致密的氧化膜;
② B元素的原子序数比A元素大,其原子的次外层的电子数是最外层电子数的2倍;
③ E与A同周期,C、D、E三种元素形成的单质或化合物可发生如下图所示的反应。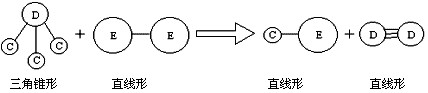
请回答下列问题
(1)写出A元素的单质与NaOH溶液反应的化学方程式;
(2)B元素在元素周期表第周期第族;
B的固态氧化物的晶体类型是;
(3)D元素的原子结构示意图是;
(4) B元素与E元素的最高价氧化物的水化物的酸性强弱>(写化学式);
(5)写出元素E的单质与NaOH溶液反应的离子方程式。