化学平衡移动原理,同样也适用于其他平衡,已知在氨水中存在下列平衡:
NH3+H2O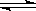 NH3·H2O
NH3·H2O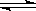 NH4++OH-
NH4++OH-
(1)向氨水中加入MgCl2固体时,平衡向______反应方向移动,现象为____________。
(2)向氨水中通入HCl,平衡向_______反应方向移动,此时溶液中浓度减小的粒子有___________、___________、___________。
(3)向浓氨水中加入少量碱石灰,平衡向______反应方向移动,溶液pH值_________(填“增大”、“减小”或“不变”),现象为______________________。实验室常利用该原理制备氨气,在此过程中碱石灰的另一个作用是_______。
下列表示对应化学反应的离子方程式正确的是
| A.用白醋除铁锈:Fe2O3+6H+===3H2O+2Fe3+ |
| B.向NH4HCO3溶液中加入过量的Ba(OH)2溶液并加热: Ba2++ 2OH-+NH 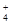 + HCO + HCO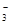 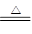 NH3↑+2H2O+BaCO3↓ NH3↑+2H2O+BaCO3↓ |
C.用过量冷氨水吸收SO2:SO2+NH3·H2O===HSO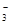 +NH +NH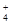 |
D.用强碱吸收工业制取硝酸尾气:NO+ NO2+2OH-===2NO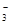 +H2O +H2O |
下列离子方程式正确的是
| A.向CuSO4溶液中投入Na: Cu2++ 2Na= Cu+ 2Na+ |
| B.向FeCl3溶液中滴加KSCN溶液: Fe3+ + 3SCN- = Fe(SCN)3↓ |
| C.向NaHCO3溶液中加过量Ca(OH)2溶液:Ca2+ + HCO3- + OH- = CaCO3↓ + H2O |
| D.向BaCO3固体中加入过量的稀H2SO4:BaCO3 + 2H+= Ba2+ + CO2↑ + H2O |
室温下,下列各组离子能大量共存的是
| A.稀硫酸中:K+、Mg2+、AlO2-、S2O32- |
| B.Na2S溶液中:SO42-、K+、Cl-、Cu2+ |
C. =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42- =10-13mol·L-1溶液中:Fe3+、NH4+、Mg2+、 SO42- |
| D.通入大量CO2的溶液中:Na+、ClO-、CH3COO-、HCO3- |
三氟化氮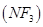 是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应:3NF3+5H2O=2NO+HNO3+9HF。下列有关该反应的说法正确的是
是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应:3NF3+5H2O=2NO+HNO3+9HF。下列有关该反应的说法正确的是
| A.NF3是氧化剂,H2O是还原剂 |
| B.NF3在潮湿空气中泄漏会看到红棕色气体 |
| C.每消耗0.2mol氧化剂,可收集到5.418L气体 |
| D.若生成1molHNO3,则转移NA个电子 |
设NA代表阿伏加德罗常数的值,下列说法中正确的是
| A.1L 1mol·L-1的CH3COOH溶液中含有NA个氢离子 |
| B.含NA个Na+的Na2O溶解于1L水中,Na+的物质的量浓度为1mol·L-1 |
| C.0.1mol金属钠在过量氧气中充分燃烧,生成的化合物中离子总数为0.15NA |
D.VLCO和NO的混合气体中含有的氧原子个数为 |