某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写)______________________.
(2)上述(B)操作的目的是___________________________________。
(3)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)_________________________。
(4)实验中用左手控制_________(填仪器及部位),眼睛注视_______,直至滴定终点。判断到达终点的现象是___________。
(5)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对测定结果的影响是___________________________________。
(6)滴定结束后如仰视观察滴定管中液面刻度,则对滴定结果的影响是______。
实验室用乙醇和浓硫酸共热制取乙烯,常因温度过高而生成少量的二氧化硫,有人设计下列实验以确认上述混和气体中有乙烯和二氧化硫。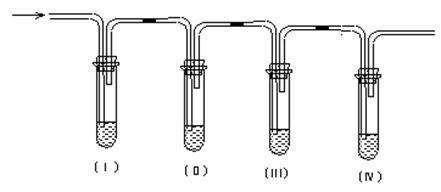
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ装置可盛放的试剂是:I;II;III;IV(将下列有关试剂的序号填入空格内);
| A.品红溶液 | B.氢氧化钠溶液 | C.浓硫酸 | D.酸性高锰酸钾溶液 |
(2)能说明二氧化硫气体存在的现象是 ______________________________________;
(3)使用装置Ⅱ的目的是 _________________________________________________ ;
(4)使用装置Ⅲ的目的是___________________________________________________;
(5)确证含有乙烯的现象是_________________________________________________。
50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: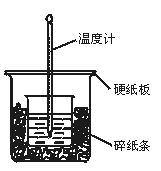
(1)从实验装置上看,图中尚缺少的一种玻璃用品是。
(2)烧杯间填满碎纸条的作用是。
(3)大烧杯上如不盖硬纸板,求得的中和热数值(填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”“不相等”),所求中和热(填“相等”“不相等”),简述理由:。
用质量分数为98%,密度为1.84g· cm-3的浓硫酸配制250mL物质的量浓度为2mol·L-1的稀硫酸。
(1)需要使用的主要仪器有量筒、烧杯、玻璃棒、、。
(2)其操作步骤可分解为以下几步:
A.用量筒量取mL浓硫酸,(简述浓硫酸的稀释操作),冷却
B.用蒸馏水洗涤烧杯和玻璃棒2~3次,将每次的洗涤液都转移入容量瓶里
C.将稀释后的硫酸小心地用玻璃棒引流至容量瓶里
D.检查250mL容量瓶是否漏水
E.将蒸馏水直接加入容量瓶至刻度线以下2cm处
F.盖紧瓶塞,上下倒转摇匀溶液
G.用胶头滴管向容量瓶里逐滴加入蒸馏水,到凹液面最低点恰好与刻度线相切
请据此填写:
①完成上述步骤中的空白处。
②正确的操作顺序是(用字母填写):
()→( )→( )→ B →( )→()→()
③进行A步操作时,选用量筒的规格是。(选填字母)
A.10mL B.50mLC.100mL D.1000mL
④下列情况对所配制的稀硫酸浓度有何影响?(选填“偏高”、“偏低”、“无影响”)。
A.用量筒量取浓硫酸时仰视,配制的稀硫酸浓度将
B.容量瓶用蒸馏水洗涤后残留有少量的水_________
C.定容时仰视溶液的凹液面 _________
在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命。下表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
| 成分 |
质量(g) |
摩尔质量(g ·mol-1) |
| 蔗糖 |
25.00 |
342 |
| 硫酸钾 |
0.25 |
174 |
| 阿司匹林 |
0.17 |
180 |
| 高锰酸钾 |
0.25 |
158 |
| 硝酸银 |
0.02 |
170 |
(1)下列“鲜花保鲜剂”的成分中,属于非电解质的是________。
A.蔗糖 B.硫酸钾 C.高锰酸钾 D.硝酸银
(2)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为_______ mol/L。(注意:只要求用原始数据写出数学表达式,不需要化简与计算)
(3)配制上述“鲜花保鲜剂”所需的仪器有:电子天平、药匙、烧杯、量筒、玻璃棒、______________、_______________。(在横线上填写所缺仪器的名称)
(4)在溶液配制过程中,下列操作对配制结果没有影响的是___________。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚刚配制完一定物质的量浓度的NaCl溶液而未洗净
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
如图为实验室制取蒸馏水的装置示意图,根据图示回答下列问题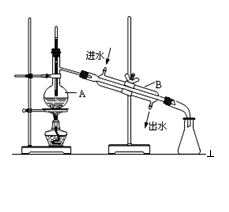
(1)图中明显的两处错误是
①_________________________________________
②_________________________________________
(2)A仪器的名称是______________,B仪器的名称是_______________。
(3)实验时A中除加入自来水外,还需加入少量__________,其作用是________________。