读下列药品标签,有关分析不正确的是( )
| 选项 |
A |
B |
C |
D |
| 物品标签 |
 |
药品:××× |
 |
 |
| 分析 |
该试剂应该装在橡胶塞的细口瓶中 |
该药品不能与皮肤直接接触 |
该物质受热易分解 |
该物质浓度为18.4mol/L |
A.A B.B C.C D.D
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能),下列叙述正确的是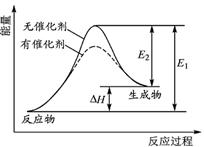
| A.该反应为放热反应 |
| B.催化剂能改变反应的焓变 |
| C.催化剂能降低反应所需活化能,增加活化分子百分数 |
| D.逆反应的活化能大于正反应的活化能 |
下列说法中可以说明密闭容器中的反应:P(g)+Q(g) R(g)+S(g)在恒温下已达平衡状态的是
R(g)+S(g)在恒温下已达平衡状态的是
| A.反应容器内压强不随时间而变化 |
| B.P和S的生成速率相等 |
| C.反应容器内P、Q、R、S四者共存 |
| D.反应容器内总物质的量不随时间而变化 |
我国燃煤锅炉大多是采用沸腾炉(注:通过空气流吹沸使煤粉在炉膛内呈“沸腾状”燃烧),采用沸腾炉的好处是
| A.增大煤燃烧时的燃烧热并形成清洁能源 |
| B.减少煤中杂质气体(如SO2)的形成 |
| C.使煤炭充分燃烧,杜绝CO的排放 |
| D.使燃料燃烧充分,从而提高燃料的利用率 |
下列溶液中,各微粒的物质的量浓度关系正确的是
| A.室温下,向0.01 mol·L-1的NH4HSO4溶液中滴加NaOH溶液至中性:C(Na+)>C(SO42-)>C(NH4+)>C(OH-)=C(H+) |
| B.0.1 mol·L-1的NaHCO3溶液:C(Na+)>C(OH-)>C (HCO3-)>C(H+) |
| C.Na2CO3溶液:C(OH-)-C(H+)=C(HCO3-)+C(H2CO3) |
| D.25℃时,浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液,呈酸性:C(CH3COO-)+C(OH-)<C(CH3COOH)+C(H+) |
常温下,下列各组离子一定能大量共存的是
| A.在由水电离出的C(H+)=10-13 mol·L-1的溶液中:NH4+、Na+、Cl-、AlO2- |
| B.在强碱性溶液中:Na+、K+、CO32-、NO3- |
| C.在pH=12的溶液中:NH4+、Na+、SO42-、Cl- |
| D.在C(H+)=0.1 mol·L-1的溶液中:K+、I-、Cl-、NO3- |