羰基硫(COS)可作为一种蚜虫熏蒸剂,能防止某些昆虫、线虫和蚜虫的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g) COS(g)+H2(g) K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是( )
COS(g)+H2(g) K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是( )
| A.升高温度,H2S浓度增加,表明该反应是吸热反应 |
| B.通入CO后,正反应速率逐渐增大 |
| C.CO的平衡转化率为80% |
| D.反应前H2S物质的量为7mol |
等质量的两份锌粉a和b,分别加入过量的稀硫酸中,a中同时加入少量CuSO4溶液,下列各图中表示其产生氢气总体积(V)与时间(t)的关系正确的是
一定温度下反应N2(g)+3H2(g)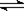 2NH3(g)达到化学平衡状态的标志是
2NH3(g)达到化学平衡状态的标志是
| A.单位时间里每增加1molN2,同时减少2molNH3 |
| B.c(N2)∶c(H2)∶c(NH3)=1∶3∶2 |
| C.N2与H2的物质的量与NH3的物质的量相等 |
| D.N2、H2和NH3的质量分数不再改变 |
已知在25℃、1.0×105Pa条件下,2mol氢气燃烧生成水蒸气放出484KJ热量,下列热化学方程式正确的是
| A.H2O(g)==H2(g)+1/2 O2(g) △H=+242 kJ/mol |
| B.2H2(g)+O2(g)===2H2O(l) △H=-484kJ/mol |
| C.H2(g)+1/2 O2(g)==H2O(g) △H=+242kJ/mol |
| D.2H2(g)+O2(g)==2H2O(g) △H=+484 kJ/mol |
人造地球卫星上使用的一种高能电池——银锌蓄电池,其电池的电极反应式为:
Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是
| A.负极,被氧化 | B.正极,被还原 |
| C.负极,被还原 | D.正极,被氧化 |
在体积为1 L的密闭容器中(体积不变)充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
CH3OH(g)+H2O(g)。测得CO2和CH3OH(g)的浓度随时间变化如图所示。下列说法正确的是
| A.进行到3分钟时,正反应速率和逆反应速率相等 |
| B.10分钟后容器中各物质浓度不再改变 |
| C.达到平衡后,升高温度,正反应速率增大、逆反应速率减小 |
| D.3min前v正>v逆,3min后v正<v逆 |